En 1897 Eduard Büchner (químico, invento los embudos Büchner) trabajo con levaduras y lo que él describió es que si uno tritura las levaduras rompiendo todas las células y hace un extracto de eso, ese extracto aun tienen la capacidad de transformar el azúcar en alcohol. Fue él el que dijo que esta capacidad de catalizar estas reacciones químicas las tienen ciertos compuestos que las tienen las levaduras, pero no es necesario que la levadura esté viva, es algo independiente, que queda, y eso lo llamo fermento.
En 1926 James Samner, por primera vez, logró purificar un fermento y cristalizarlo, la ureasa, la primera enzima que se obtuvo de forma cristalizada, la analizó y encontró que tenia la composición de una proteína. Posteriormente se cristalizaron mas enzimas y en todas se encontró que tenían una estructura similar a las proteínas.
Las enzimas tienen mucha importancia simplemente por todos sus usos y aplicaciones:
· Doméstico: detergentes (removiendo la suciedad)
· Clínica:
· Biología molecular: DNA (clonación, replicación de DNA)
· Medicina: comprensión de ciertos problemas metabólicos
Se descubrió las riboenzimas, que son moléculas de RNA que catalizan reacciones químicas relacionadas con RNA y DNA.
Sin embargo en este capítulo de enzimas, nos referiremos a la forma clásica.
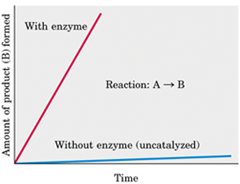 Acá tenemos un gráfico en función del tiempo que cuantifica la cantidad de producto de una reacción en donde a partir de A se forma B. Entonces acá se representa como aumenta la cantidad de B en el tiempo cuando no está la enzima, o sea, cuando la reacción no está catalizada y por otra parte tenemos la reacción catalizada con la enzima, demostrándose que la pendiente cambia drásticamente. Para obtener la velocidad de reacción hay que sacar la pendiente de la curva.
Acá tenemos un gráfico en función del tiempo que cuantifica la cantidad de producto de una reacción en donde a partir de A se forma B. Entonces acá se representa como aumenta la cantidad de B en el tiempo cuando no está la enzima, o sea, cuando la reacción no está catalizada y por otra parte tenemos la reacción catalizada con la enzima, demostrándose que la pendiente cambia drásticamente. Para obtener la velocidad de reacción hay que sacar la pendiente de la curva. En la realidad para casi todas las enzimas que participan en metabolismo, cuando éstas no están presentes, la velocidad es casi imperceptible por lo que la pendiente que se muestra en la figura está exagerada, porque prácticamente no ocurren.
¿Cómo actúan los catalizadores?
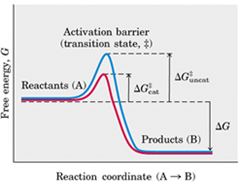 Esta imagen es válida para los catalizadores biológicos y los que no, que hace que la velocidad de reacción aumente, actúa de esta forma:
Esta imagen es válida para los catalizadores biológicos y los que no, que hace que la velocidad de reacción aumente, actúa de esta forma:Aquí se muestra que entre un reactante, se sigue con el ejemplo anterior, A y el producto B existe una barrera energética, energía libre en función de una coordenada, que acá se llama coordenada de reacción (de la reacción entre A y B). Siempre se usa este método de hablar de una coordenada de reacción, para no comprometer con cual es el parámetro que se está midiendo.
Como podemos apreciar, para trasformar el reactante A en productos B es necesario pasar por una barrera energética, un estado de transición. Y la función del catalizador es disminuir la barrera o energía de activación, pero no afecta el G de la reacción, y por lo tanto tampoco afecta la constante de equilibrio, sólo aumenta la velocidad de reacción reduciendo esa barrera, esto uno se lo tiene que imaginar de forma que para que el reactante pueda llegar a producto tienen que llegar a este estado de alta energía, entonces de todas la moléculas de reactante que hay, no todas tienen la misma energía en un momento dado, sino que hay una distribución de energía, y solamente las que tengan la energía igual a la barrera de activación son las que pueden reaccionar en este momento, luego en otro momento, otras moléculas son las que van a reaccionar.
Entonces, si la barrera energética es muy alta muy pocas moléculas podrán reaccionar, y como el catalizador hace que el estado de transición sea de menor energía, hay un mayor número de moléculas que tienen ese grado de energía y por lo tanto van a reaccionar. Entonces cuando una reacción ocurre con catálisis el estado de transición es diferente, y es igual para catálisis química como biológica.
En general, un catalizador químico como biológico, no se consume en la reacción, en realidad no reacciona, cataliza. Además un catalizador puede catalizar la reacción inversa de la misma forma como catalizo la reacción inicial.
Las enzimas tienen ciertas diferencias con los catalizadores químicos:
· Mayor poder catalítico que los catalizadores químicos
· Especificidad
· Actúan en condiciones “suaves” de temperatura, pH, presión atmosférica.
· Sufren regulación, pueden ser activadas, que catalizan mejor, o desactivadas, que catalicen menos o simplemente no catalizan.
 Acá tenemos el ejemplo de la Citofilina que tiene un factor de velocidad de reacción 105 respecto de la reacción sin la Citofilina; la Anhidrasa carbónica con un factor de 107, que participa la síntesis de:
Acá tenemos el ejemplo de la Citofilina que tiene un factor de velocidad de reacción 105 respecto de la reacción sin la Citofilina; la Anhidrasa carbónica con un factor de 107, que participa la síntesis de:CO2 + H2O H2CO3 H+ + HCO3-
Ahora un ejemplo de de especificidad:
La Glutamina sintetasa que cataliza la síntesis de Glutamina a partir de L-Glutamato, diferenciando de D-Glutamato y reemplazando un grupo amido en el acido carboxílico en la cadena lateral, para transportar NH4+ hacia el hígado y riñones por la sangre.
Otro caso de especificidad son las porteasas o enzimas proleolíticas, que son las enzimas que catalizan la hidrólisis de enlaces peptídicos. Existen proteasas de diferente especificidad.
Ejemplo:
1-2-3-n - (n+1)-…
Entonces aquí se considera el enlace peptídico entre los residuos n y (n+1), de color rojo, que puede sufrir hidrólisis.
Existen proteasas de diferente especificidad:
· Tripsina: enzima que proviene del páncreas y cataliza la hidrólisis si n es Lisina o Arginina (aminoácidos básicos).
· Quimotripsina: cataliza la hidrólisis si n es Triptófano, Tirosina, Fenilalanina, Leucina ó Metionina (aminoácidos apolares), siendo menos específica que la Tripsina, debido a la gran variedad que puede catalizar.
· Trombina: cataliza el último paso que tiene relación con la coagulación de sangre. Ésta cataliza la hidrólisis si n es Arginina y (n+1) es Glicina, o sea, debe haber cierta secuencia, siendo más específica que la Tirosina.
Existe una enzima proteolítica que practicamente no tiene especificidad, la Subtilizina (se obtiene de unos bacilos que viven en el suelo), que hidroliza todos los enlaces peptídicos. Pero aun tiene especificidad ya que solo hidroliza enlaces peptídicos y no cualquier enlace.
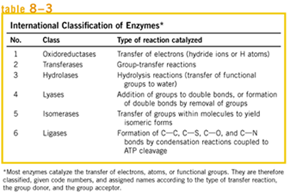
Existe una clasificacion de las enzimas de acuerdo al tipo de acción:
Ejemplo:
La enzima que cataliza la siguiente reacción:
ATP + glucosa ADP + glucosa-6-fosfato *primera reacción de la glicólisis
Esta enzima tiene como nombre no sistemático Hexoquinasa.
Si uno quiere clasificar esta enzima debe hacerlo de la siguiente manera:
· Tipo de reacción: Transferasa
· Clasificación de la enzima: Clase Nº 2
· Nombre sistemático: ATP-glucosa-fosfo-transferasa
· Nº de la enzima: 2.7.1.1
Hay que dejar en claro que las mismas enzimas de diferentes especies no son iguales, aunque tengan el mismo número, también importa el origen.
Ejemplos de nombres no sistemáticos:
· Ureasa, amilasa, Fructosa bifosfatasa, que aluden al sustrato, o sea, actúan sobre la urea, fructosa bifosfato, etc.
· Arginina sintetasa (síntesis de Arginina), Histidina descarboxilasa (descarboxilación de Histidina) que aluden a la reacción.
· Subtilisina, tripsina que aluden a otros orígenes.
Cofactores
Componentes no proteicos que ciertas enzimas necesitan para tener actividad catalítica, sin el cofactor no hay catálisis. Como el cofactor no es proteico, no posee cadena polipeptídica. Existen los cofactores inorgánicos y otros orgánicos ó coenzimas. Algunos cofactores son grupos prostéticos de la enzima. El concepto de grupo prostético corresponde a un componente no proteico pero que se encuentra firmemente unido a la cadena polipeptídica, formando parte de la proteína, pero no es un aminoácido.
Ejemplo de cofactores:
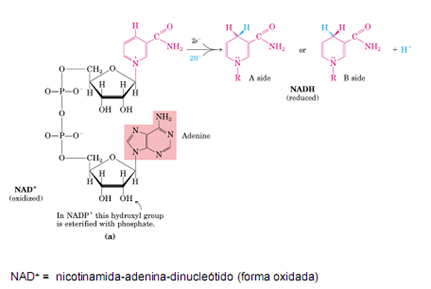
Las coenzimas de óxido-reducción NAD+/NADH y NADP+/NADPH
Se muestra una reacción en donde ésta actúa como coenzima recibiendo electrones, y se forma la forma reducida NADH.
Catálisis enzimática:
Acá los reactantes se les llama sustrato.
La enzima no actúa a distancia, sino que, cuando la enzima cataliza la reacción, el sustrato se une a la enzima formando el complejo enzima-sustrato (ES).
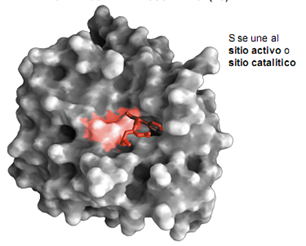
En la figura podemos apreciar una enzima y en rozado el sitio activo o sitio catalítico, en la estructura tridimensional existe un sitio especifico al cual se une el sustrato, en este caso la molécula de color rojo, formando el complejo ES.
Esta estructura tridimensional del sitio catalítico permite vislumbrar y explicar una de las características interesantes de las enzimas que es la especificidad.












0 comentarios:
Publicar un comentario