Algunas funciones que cumplen las proteínas, como por ejemplo la del transporte de oxígeno, se pueden explicar mediante las estructuras de las proteínas que participan en dichos procesos y porque la reacción ocurre de una manera y no de otra.
Las proteínas involucradas en el transporte de oxígeno son la hemoglobina y la mioglobina. La hemoglobina se encuentra presente en la sangre por lo que trasporta el oxígeno por todo el torrente sanguíneo; la hemoglobina puede estar en dos estados, desoxigenados y oxigenados.
El los estados oxigenados se pueden trasferir el oxígeno a los músculos y este a la mioglobina y entonces este 02 llega finalmente a la mitocondria donde se ocupa en la producción de energía. En el tejido muscular se produce CO2 que pasará a la sangre donde se transporta tanto como ión bicarbonato como asociado a la hemoglobina, siempre por los aminos terminales produciendose en los pulmones una menor presión parcial de CO2, y este CO2 finalmente sale y se intercambia finalmente con el O2. Estos intercambios de gases estan intimamente ligados a la estructura y las características estructurales de las proteínas.
Los glóbulos rojos son células bastante especiales ya que son anucleadas (que no poseen núcleo) y en el fondo corresponden a una verdadera bolsa de hemoglobina, también casi no posee organelos esto es en humanos porque en la mayoría de los vertebrados los glóbulos rojos son nucleados.
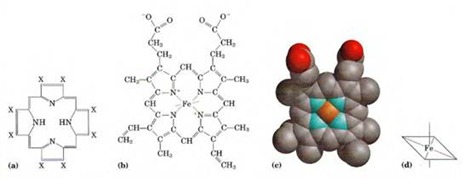
La hemoglobina posee una estructura cuaternaria (es un heterotetrámero con dos cadenas alfa y dos cadenas beta). También posee un grupo hemo que es de vital importancia para el transporte de oxígeno. El grupo hemo posee unos anillos pirrólicos y los nitrógenos permiten coordinar un átomo de fierro (+2). El fierro puede tener 6 enlaces de coordinación, 4 de ellos están con los nitrógenos de los anillos pirrólicos y una histidina si ahora participa las proteínas de una de las globinas y es capaz de coordinar un quinto del estado de valencia del fierro y la sexta se utiliza para coordinar el O2.
La hemoglobina puede estar en dos estados de oxidación con Fe+2 y Fe+3, en donde el fierro cuando se oxida a Fe+3 es muy difícil volverlo a reducir. La hemoglobina se puede oxigenar fácilmente por lo que se puede dilucidar cual sangre esta o no oxigenada; la sangre desoxigenada es de color roja a azul, e cambio la sangre oxigenada es de un rojo vivo granate.
La sangre azul como se le llama a la sangre de las familias reales corresponde a sangre poco oxigenada.
Así como el CO2 puede unirse a la hemoglobina, el monóxido de carbono también es capaz de unirse al grupo hemo de la hemoglobina formando carboxi hemoglobina.
La afinidad del CO es alrededor de 230 veces mayor que el O2. Esto explica por que en monóxido de carbono es tan tóxico ya que al igual que el O2 se puede unir al grupo hemos de la hemoglobina. El hecho de que el grupo hemo esté inserto en la hemoglobina ayuda a que 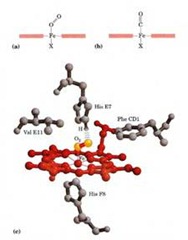 esa extremadamente alta afinidad del CO por el grupo hemo baje considerablemente. Además de la histidina que ayuda a coordinar al fierro en su posición. El CO tiende a formar un enlace recto con respecto al oxígeno y este ultimo cuando se une forma un ángulo bajo condiciones normales ya que la histidina obliga al CO a doblarse por lo que cambia su conformación espacial en la unión con el grupo hemos (un dobles forzado) por lo que la afinidad del CO disminuye. La importancia de la histidina radica es que impide que trazas de CO se puedan unir de forma irreversible al grupo hemo (histidina distal).
esa extremadamente alta afinidad del CO por el grupo hemo baje considerablemente. Además de la histidina que ayuda a coordinar al fierro en su posición. El CO tiende a formar un enlace recto con respecto al oxígeno y este ultimo cuando se une forma un ángulo bajo condiciones normales ya que la histidina obliga al CO a doblarse por lo que cambia su conformación espacial en la unión con el grupo hemos (un dobles forzado) por lo que la afinidad del CO disminuye. La importancia de la histidina radica es que impide que trazas de CO se puedan unir de forma irreversible al grupo hemo (histidina distal).
 esa extremadamente alta afinidad del CO por el grupo hemo baje considerablemente. Además de la histidina que ayuda a coordinar al fierro en su posición. El CO tiende a formar un enlace recto con respecto al oxígeno y este ultimo cuando se une forma un ángulo bajo condiciones normales ya que la histidina obliga al CO a doblarse por lo que cambia su conformación espacial en la unión con el grupo hemos (un dobles forzado) por lo que la afinidad del CO disminuye. La importancia de la histidina radica es que impide que trazas de CO se puedan unir de forma irreversible al grupo hemo (histidina distal).
esa extremadamente alta afinidad del CO por el grupo hemo baje considerablemente. Además de la histidina que ayuda a coordinar al fierro en su posición. El CO tiende a formar un enlace recto con respecto al oxígeno y este ultimo cuando se une forma un ángulo bajo condiciones normales ya que la histidina obliga al CO a doblarse por lo que cambia su conformación espacial en la unión con el grupo hemos (un dobles forzado) por lo que la afinidad del CO disminuye. La importancia de la histidina radica es que impide que trazas de CO se puedan unir de forma irreversible al grupo hemo (histidina distal). La estructura de la hemoglobina esta compuesta por subunidades alfa y beta las que a su vez están formadas por 8 alfa hélices, ambas cadenas alfa y beta solo se diferencian por unos cuantos aminoácidos de sus cadenas primarias. Toda la parte hidrofóbica del grupo hemos esta inserta en el centro de la proteína.
La proteína fija con los distintos enlaces de coordinación el grupo hemo dentro de la molécula y a su vez reducir la afinidad del CO.
Si se mide la unión de distintas concentraciones de oxígeno a la hemoglobina, en la figura esta expresado como presiones de O2 como es un gas, se va midiendo con concentraciones de O2 cada vez mayores, lo que nos muestra de que cuando todos los grupos hemos esta unidos con O2, la proteína esta saturada y en función de eso se puede saber cuanto oxígenos lleva la hemoglobina.
Para la mioglobina una pequeña concentración de O2 satura rápidamente a la proteína y en cambio la hemoglobina la tendencia es distinta ya que a bajas concentraciones de O2 casi no se une a la proteína y al aumentar a una cierta cantidad empieza a aumentar la unión O2-hemoglobina hasta que rápidamente llega a la saturación (el O2 comienza a unirse en un principio con lentitud pero luego se dispara la unión del O2 a la hemoglobina). De las curvas se puede inferir la afinidad de cada molécula por el O2; como la concentración con la cual se satura el 50% de la proteína, lo que corresponde a una medida de la afinidad con que se une el O2 al grupo hemo. Para la hemoglobina tiene una afinidad de alrededor de 26 m torr y la mioglobina tiene una valor de 2, lo que significa que la mioglobina es mucho más afín por el O2 que la hemoglobina esto significa que a una menor concentración de O2 la mioglobina se satura más rápidamente que la hemoglobina. El sentido Fisiológico de este comportamiento radica en que si bien es cierto la hemoglobina le traspasa el O2 a la mioglobina, pero si la hemoglobina tuviera una mayor afinidad por el O2 no seria capaz de cedérselo a la mioglobina, la mioglobina se quedaría estonces desoxigenada y por lo tanto también el músculo sin ser capaz de producir energía.
La curva de la hemoglobina es sigmoidea, se debe a que la hemoglobina es un tetrámero y la de la mioglobina es hiperbólica. Estas curvas reflejan de que existe una coperatividad entra las subunidades. Si las dos tuvieran una curva hiperbólica la proteína transportadora hemoglobina seria eficiente en la unión pero ineficiente en la descarga de O2. En la curva sigmoidea la proteína transportadora es ineficiente en la unión y eficiente en la descarga.
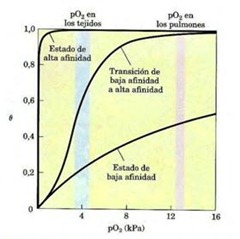
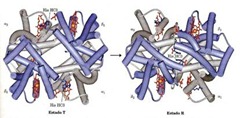 La explicación de la curva sigmoidea es la siguiente: existen dos modelos, uno de ellos es el modelo Monod, Wyman y Changeux, llamado también modelo concertado y el modelo de Koshland o modelo secuencial; la hemoglobina puede estar en dos estados conformacionales, un estado T (tenso) y en estado R (relajado). Cuando la subunidad esta en estado R es mucho más afín, es decir, tiene una unión mucho más fuerte por el O2 que cuando está en estado T, que es un estado de unión más débil. El resultado de los dos modelos es exactamente el mismo, la hemoglobina sin el O2 unido implica que todas las subunidades se encuentran en estado T, entonces cuando el oxígenos empieza a ocupar las uniones fuertes invita a la subunidad vecina a cambiar de forma (induciendo un cambio conformacional) al estado de unión fuerte lo que promueve la unión del O2. Esto explica por qué a bajas concentraciones casi no se une el O2 pero debido a esta promoción todas las subunidades se van trasformando a un estado R. En resumen las subunidades pueden estar en estado T o R pero al unirse una molécula de O2 al estado T, desplaza todas al estado R por lo que el O2 se une rápidamente. Esto mismo produce que la proteína sea mucho más eficiente para transportar el O2 y llevarla al músculo y podérsela transferir a la mioglobina para que la lleve al interior de la célula muscular precisamente a la mitocondria, para que ésta la pueda utilizar en la producción de energía.
La explicación de la curva sigmoidea es la siguiente: existen dos modelos, uno de ellos es el modelo Monod, Wyman y Changeux, llamado también modelo concertado y el modelo de Koshland o modelo secuencial; la hemoglobina puede estar en dos estados conformacionales, un estado T (tenso) y en estado R (relajado). Cuando la subunidad esta en estado R es mucho más afín, es decir, tiene una unión mucho más fuerte por el O2 que cuando está en estado T, que es un estado de unión más débil. El resultado de los dos modelos es exactamente el mismo, la hemoglobina sin el O2 unido implica que todas las subunidades se encuentran en estado T, entonces cuando el oxígenos empieza a ocupar las uniones fuertes invita a la subunidad vecina a cambiar de forma (induciendo un cambio conformacional) al estado de unión fuerte lo que promueve la unión del O2. Esto explica por qué a bajas concentraciones casi no se une el O2 pero debido a esta promoción todas las subunidades se van trasformando a un estado R. En resumen las subunidades pueden estar en estado T o R pero al unirse una molécula de O2 al estado T, desplaza todas al estado R por lo que el O2 se une rápidamente. Esto mismo produce que la proteína sea mucho más eficiente para transportar el O2 y llevarla al músculo y podérsela transferir a la mioglobina para que la lleve al interior de la célula muscular precisamente a la mitocondria, para que ésta la pueda utilizar en la producción de energía. ¿Cómo ocurren los cambios conformacionales en las proteínas?
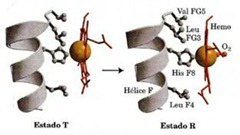 La estructura de las proteínas se puede determinar bajo distintas condiciones, la estructura de la hemoglobina se ha determinado como oxi hemoblobina y como desoxi hemoglobina. Cuando se une el O2 tira al ión Fe, de modo que este quede mas coplanar con el anillo de la protoporfirina, se produce un cambio en la movilidad de la hemoglobina y a su vez tira de la histidina, por lo que hace que cada subunidad cambie y produce que toda la proteína sufra un cambio. Estos cambios ocurren por que la estructura cuaternaria esta mantenida por enlaces débiles, como puentes de hidrógeno, fuerzas de Van der Walls y enlaces iónicos, los cuales son los más importantes en la hemoglobina. La transición del estado T al R esta provocada por cambios en las posiciones de cadenas laterales de aminoácidos clave como la valina, el ácido aspártico y la argenina que rodean al grupo hemo. En el estado T la porfirina esta ligeramente curvada, provocando que el Fe del grupo hemo sobresalga ligeramente hacia la histidina proximal. La unión del O2 hace que el grupo hemo adquiera una estructura más coplanar cambiando la posición de la histidina proximal y de la hélice unida.
La estructura de las proteínas se puede determinar bajo distintas condiciones, la estructura de la hemoglobina se ha determinado como oxi hemoblobina y como desoxi hemoglobina. Cuando se une el O2 tira al ión Fe, de modo que este quede mas coplanar con el anillo de la protoporfirina, se produce un cambio en la movilidad de la hemoglobina y a su vez tira de la histidina, por lo que hace que cada subunidad cambie y produce que toda la proteína sufra un cambio. Estos cambios ocurren por que la estructura cuaternaria esta mantenida por enlaces débiles, como puentes de hidrógeno, fuerzas de Van der Walls y enlaces iónicos, los cuales son los más importantes en la hemoglobina. La transición del estado T al R esta provocada por cambios en las posiciones de cadenas laterales de aminoácidos clave como la valina, el ácido aspártico y la argenina que rodean al grupo hemo. En el estado T la porfirina esta ligeramente curvada, provocando que el Fe del grupo hemo sobresalga ligeramente hacia la histidina proximal. La unión del O2 hace que el grupo hemo adquiera una estructura más coplanar cambiando la posición de la histidina proximal y de la hélice unida.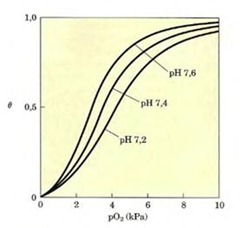 Existe otras causas que producen cambios conformacionales en la estructura de la hemoglobina y uno de ellos es lo que se denomina el efecto Borh; el rompimiento de un puente de hidrógeno en la hemoglobina hace que se libere un protón lo cual produce que localmente se disminuya el pH, lo que provoca que baje la afinidad global de la hemoglobina por el oxígeno, es decir, cambia al estado T, lo que promueve que se suelte más facil el O2. Esto tiene una relación con la actividad muscular, ya que como se libera más oxigeno, baja la afinidad por el oxigeno, por lo tanto el intercambio es mejor y además se esta produciendo CO2 en el músculo y el aumento de CO2 tiende llevar a la hemoglobina hacia el estado conformacional T y por lo que se puede unir el CO2 a los grupo amino terminales y toda la proteína se mueve hacia una mayor liberación de O2 y el músculo en ejercicio esta liberando mas CO2, por lo que hay una concentración local de CO2 mas alta y un pH ligeramente más bajo. Ambas condiciones favorecen, o mejoran la liberación de O2. Hablamos de cómo modular la eficacia con que trabaja esta macromolécula, siendo este aspecto muy importante y esa modulación de nuevo tiene que ver con un cambio conformacional de la proteína. El cambio de la distribución espacial de sus residuos, que afectan obviamente la zona donde se une el O2 con el grupo hemo y eso hace que cambie la afinidad.
Existe otras causas que producen cambios conformacionales en la estructura de la hemoglobina y uno de ellos es lo que se denomina el efecto Borh; el rompimiento de un puente de hidrógeno en la hemoglobina hace que se libere un protón lo cual produce que localmente se disminuya el pH, lo que provoca que baje la afinidad global de la hemoglobina por el oxígeno, es decir, cambia al estado T, lo que promueve que se suelte más facil el O2. Esto tiene una relación con la actividad muscular, ya que como se libera más oxigeno, baja la afinidad por el oxigeno, por lo tanto el intercambio es mejor y además se esta produciendo CO2 en el músculo y el aumento de CO2 tiende llevar a la hemoglobina hacia el estado conformacional T y por lo que se puede unir el CO2 a los grupo amino terminales y toda la proteína se mueve hacia una mayor liberación de O2 y el músculo en ejercicio esta liberando mas CO2, por lo que hay una concentración local de CO2 mas alta y un pH ligeramente más bajo. Ambas condiciones favorecen, o mejoran la liberación de O2. Hablamos de cómo modular la eficacia con que trabaja esta macromolécula, siendo este aspecto muy importante y esa modulación de nuevo tiene que ver con un cambio conformacional de la proteína. El cambio de la distribución espacial de sus residuos, que afectan obviamente la zona donde se une el O2 con el grupo hemo y eso hace que cambie la afinidad. Otra molécula que también es importante en es metabolismo, es la 2-3-fosfoglicerato todos los glóbulos rojos tienen 2-3-fosfoglicerato, esta molécula también tiende a que la hemoglobina se valla a un estado T y facilita la entrega de O2, ya que le baja la afinidad en esa zona.
Existen situaciones extremas en que incluso la hemoglobina sin nada de fosfoglicerato puede perder totalmente la operatividad.
El fosfoglicerato interactúa con todas las cadenas por lo tanto mantiene toda la estructura en una cierta conformación en donde se favorece mucho más la operatividad, para que realmente se mantenga la curva sigmoidea.
El fosfoglicerato en la sangre de los bancos de sangre (en los hospitales) se va perdiendo y le agregan nocina para mantener los niveles de fosfoglicerato y evitar que se pierdan, por que una vez que se pierden es de forma irreversible, por lo que cuesta mucho volver la hemoglobina a su estado con fosfoglicerato y es importante para las transfusiones, seria malo que nos pongan sangre con hemoglobina que 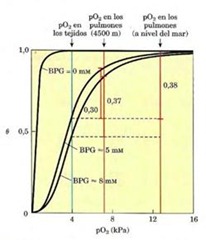 no sirve.
no sirve.
 no sirve.
no sirve. Sin fosfoglicerato se empieza a perder la coperatividad pero cuando agregamos más fosfoglicerato, se mejora la coperatividad y se puede soltar el O2 a más baja presión. Aquí en la figura donde se muestran las curvas de lo que precisamente le ocurre a las personas. La presión de O2 a nivel del mar, la presión a los 4500 metros. Esto es sin fosfoglicerato donde se pierde la coperatividad, la concentración normalmente es 5 mili molar de fosfoglicerato y 8 mili molar a grandes altitudes. Observe que la hemoglobina se une al O2 muy fuertemente en ausencia de fosfoglicerato, presentando una curva de unión hiperbólica. A nivel del mar, la hemoglobina esta casi saturada con oxígeno en los pulmones, pero su nivel de saturación es solo de un 60% en los tejidos, de manera que la cantidad de O2 liberado en los tejidos es cercana al 40% del máximo del que puede ser transportado por la sangre. A grandes altitudes la liberación de O2 disminuye en una cuarta parte, alcanzando como máximo el 30%. Un aumento en la concentración de fosfoglicerato disminuye la afinidad de la hemoglobina por el O2 haciendo que se libere a los tejidos, cerca del 40% del que transporta.
La hemoglobina fetal es distinta; tiene las cadenas alfa, pero tiene unas cadenas gama. El feto esta a una menor presión de O2 que la madre debido a que si bien es cierto la hemoglobina de la madre esta circulando, pero hay una barrera placentaria que tiene que atravesar , y al otro lado esta circulando la sangre del feto, por lo tanto la hemoglobina de la madre tiene que tener una afinidad adecuada pero la del feto tiene que tener una mucho mejor afinidad, sino jamás “agarraría” O2 y no se desarrollaría y eso es lo que ejemplifica por que tiene estas cadenas gama.
El feto que tiene, por así decirlo un estado T y un estado R distinto al de la madre justamente para que el O2 pueda ser traspasado desde la sangre materna a la sangre fetal, y en ese caso se expresan genes distintos y lo cual cambia una vez que el bebé nace produciéndose toda una adaptación, volviendo al estado normal de dos cadenas alfa o dos cadenas beta.
Existe un tipo de anemia que se denomina anemia falciforme o tetranocítica en donde las personas expresan una hemoglobina distinta denominada S la cual tiene un aminoácido cambiado. La anemia falciforme se produce por una alteración en la estructura de la hemoglobina que queda cuando baja la tensión de O2 a que esta hemoglobina forme verdaderos agregados, formando grandes fibras, por lo tanto cambia la forma al glóbulo rojo y pasa a una forma alargada casi de hoz. La hemoglobina de las células falciformes también posee cadenas alfa y las beta, y en la cadenas beta el glutamato, en posición 6, esta sustituido por una valina (el cambio de un aminoácido). El glutamato es un aminoácido ácido por lo tanto tiene carga negativa y se cambian por una valina que no tiene carga, que es apolar, es decir, un glutamato esta cargado y esta siempre afuera ,pero cuando se cambian aminoácidos cargados por un hidrofóbico al que no le gusta el agua. La sustitución del glutamato por la valina en la posición 6 de la cadena beta que se sitúa en la superficie exterior de la molécula, produce que estos puntos hidrofóbicos hacen las moléculas de desoxihemoglobina S se asocien anormalmente entre ellas, formando los grandes agregados fibroso característicos de esta enfermedad.











0 comentarios:
Publicar un comentario