La Especificidad de Quimotripsina
Aquí tenemos en relación a la quimotripsina. Como cualquier proteasa, hidroliza enlaces peptídicos, pero no cualquier enlace peptídico, sino que un enlace peptídico detrás de un residuo que tenga un grupo R, cadena lateral apolar; ahí hay varias opciones, relativamente grandes y con zonas apolares, no enteramente apolares.
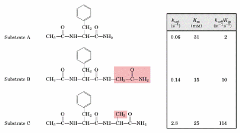
Aquí uno ve que están usando un péptido como sustrato y esta es la cadena apolar que pusieron para que se una, porque si no está un grupo mas o menos de esa índole, no hay hidrólisis y ahora tiene que estar delante del enlace peptídico, entonces el que se va a hidrolizar va a ser este (donde esta el NH2, en sustrato A)
Entonces para este sustrato (sustrato A) encontraron una baja kcat (constante catalítica), un Km de 31 mM e hicieron la razón kcat / Km que son 2.
Después con el segundo sustrato (se marca con rojo la diferencia respecto a la anterior), aquí ya le agregaron este grupo. El enlace que se va a hidrolizar en este sustrato B será NH-CH2 este es la diferencia. (Se refiere a los enlaces que se unen con el rojo)
Este segundo sustrato respecto al primero, ¿es mejor o peor?, o sea si ¿el sustrato B es mejor sustrato que sustrato A? o ¿no?, ¿si la enzima es más especifica para B que para A o mas para A que para B? R: Eso de especificidad significa que una enzima prefiere como uno dice “un sustrato frente a otro”. O sea la especificidad absoluta es que un sustrato simplemente no cataliza su reacción, eso es lo que uno se imagina, ese es el concepto que uno tiene en la cabeza de especificidad, hidroliza solamente este sustrato y el otro no; pero la cosa no es tan absoluta. Prefiere un sustrato, el otro sustrato tal vez lo transforma, pero con una eficiencia catalítica menor.
Entonces, ¿cómo se mide eso? R: Se miden los parámetros que siempre se pueden medir. ¿Cuáles son esos parámetros que se pueden medir, cuando uno estudia una enzima y un sustrato en particular? R: El Km y la kcat. El Km se obtiene gráficamente haciendo la hipérbola o se hace el grafico del reciproco de uno de los dos interceptos. Uno de los dos interceptos del grafico del reciproco da el Km y el otro intercepto da la velocidad máx.
¿Para qué sirve la velocidad máx.?, cuando la enzima esta saturada entonces uno extrapola el grafico del reciproco. O en otros términos ¿de qué depende la velocidad máx.? R: Depende de la [E] (concentración de enzimas) y de la kcat y Km para este sustrato y también para este otro sustrato. Para los tres sustratos determinan kcat y Km.
Para A y B ¿para cuál es más especifica la enzima? R: Una kcat que sea mayor indica mayor velocidad y el Km disminuye a la mitad, por estos dos datos, uno aumenta el otro disminuye. ¿Una disminución del Km es favorable o no?, ¿Indica algo favorable respecto a la especificidad o eficiencia catalítica el bajo Km? R: El Km refleja la afinidad de la enzima por el sustrato.
En ese contexto ¿qué es favorable para una alta afinidad? R: Cuando el Km es bajo, indica que el sustrato se une fuertemente, porque vasta una baja concentración para tener la mitad de la velocidad máx. Entonces sin duda el hecho del que el Km sea mas bajo es algo favorable, además la kcat es mayor, por lo tanto, aquí afecta las dos cosas; ¿entonces con qué se quedan para evaluar la situación?, ¿qué número se va usar? R: Se va usar este cuociente (kcat/Km), eso es lo que significativo.
Si se dividen estos dos números entre ellos, se llega a 2 (sustrato A) y se llega a 10 (sustrato B), o sea esto aumenta a 5 veces. 5 veces mayor especificidad para este sustrato B que el A.
En C hace otro cambio mas, le meten un CH3. ¿Dónde afecta más este único metilo?, ¿en qué parámetro si uno mira los números? R: Afecta más en la kcat de alguna manera la estabilización del estado de transición es mucho mejor para este grupo (C), entonces baja la energía de activación.
En cuanto a unión, la unión es un poco peor que para B, no se une tan bien. Pero la energía de activación baja mucho, porque eso lo refleja la kcat. Entonces con estos dos valores calculan y llegan a un valor de razón de 114 y esto obviamente es mucho mayor que 10 y mucho mayor que en 2.
Ahí uno ve claramente que si tuviera una enzima en presencia de los tres sustratos y los tres sustratos compiten con la enzima, hidrolizaría muchísimo mas a mayor velocidad este sustrato que este otro. (hidrolizaría a mayor velocidad el C)
Efecto de la Concentración de Enzima
· Vmax es directamente proporcional a [E]
Dijimos que la velocidad máx. es directamente proporcional a la [E].
Normalmente, le puse velocidad máx., porque es la situación más fácil de imaginarse. Cuando no es velocidad máx., también en realidad la velocidad depende de la [E] y normalmente es directamente proporcional, cuando es una velocidad un poquito menor que la máx.
Cuando uno quiere estudiar efectos de la [E], uno tiene que dejar todas las otras variables fijas. Entonces tiene que escoger una [S] fijo, ahí lo normal es que uno escoge una alta [S], ojala prácticamente saturada para tener altas velocidades y poder medir mejor la velocidad, porque si uno tiene baja [S] con respecto al Km, es muy difícil medir la velocidad. Entonces por eso se puso altiro velocidad máx.
· Para [E] = 0 V = 0
· Luego: el gráfico de Vmax en función de [E] es una recta que pasa por el origen.
· Se mide Vmax (o una velocidad cercana a Vmax) para determinar [E].
Cuando la [E] es cero, la velocidad es cero obviamente. Por lo tanto, ¿cómo va a ser el grafico, si uno grafica velocidad en función [E]? R: Es una recta. ¿Por dónde empieza la recta? R: La recta que empieza por el origen. Esto tiene mucha importancia, se mide la velocidad máx. o justamente una velocidad cercana a la máx., si uno no logra tener saturado la enzima es porque, tal vez no se puede usar por [S] tan altas. Esto se usa para determinar [E] y eso es algo de muchísima utilidad.
Una enzima es una proteína, entonces si uno tiene la enzima pura, uno puede usar cualquier método colorimétrico para determinar la concentración de esa enzima, como proteína. Existen varios test, son por métodos colorimétrico.
Sin embargo, si la enzima esta en la mezcla junto con otras proteínas, cuando uno mide proteínas mide proteínas totales y eso nos indica cuanta enzima hay.
Entonces con este método cuando uno mide la velocidad de la reacción catalizada uno mide cuanta enzima hay de esa enzima y no importa que esté en presencia de muchas otras proteínas y de otras componentes más, siempre y cuando no interfiera, pudiera ser que algunos interfieren. Pero en general eso permite cuantificar enzimas en muestras, eso es lo que se usa muchísimo.
De ahí se usa esta definición:
· Una unidad de actividad catalítica (U) es la cantidad de enzima que cataliza la transformación de 1 μmol de S a P por minuto, en condiciones óptimas, estandarizadas.
Se fijan entonces, ahí se cuantifica la enzima en base a su actividad catalítica.
En ensayo de actividad catalítica ¿qué es lo que mide una, en general para alguna enzima especifica? R: La velocidad de reacción; pero no es catalítica, o sea, claro por el efecto del catalizador es la velocidad de reacción. De ahí se usa la diferencia, entonces ahí se puede pasar a U. Si otro investigador, en otra parte del mundo usa la misma condición estándar, en otra muestra va a informar que hay, tales U y eso es comparable, porque son las mismas condiciones.
· Obs.: Se usan variantes de la definición para algunas enzimas, si es necesario o conveniente.
Eso de las variantes es que a veces pueden que no la U, no se defina como 1 μmol de sustrato a productos por minuto.
Hay algunos sustratos que uno no se puede cuantificar en 1 μmol; por ejemplo, cuando uno piensa en la celulasa que degradan celulosa. La celulosa es un polímero y ahí uno no lo puede cuantificar en mol, molaridad; entonces ahí hay que tener otro tipo de definición. Pero cuando se informa como se definió la U, se indica todo eso.
Efectos del pH
Aquí tenemos un caso concreto, la pepsina que es una proteasa gástrica.
Aquí tenemos el grafico:
Pepsina (proteasa gástrica)
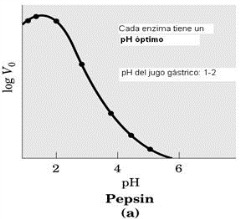 Hay que hacer un grafico logarítmico, porque cambia mucho las velocidades. Del logaritmo de la velocidad en función del pH. Si no usaron logaritmo, igual serian más o menos del mismo tipo.
Hay que hacer un grafico logarítmico, porque cambia mucho las velocidades. Del logaritmo de la velocidad en función del pH. Si no usaron logaritmo, igual serian más o menos del mismo tipo.Con el logaritmo uno comprime un poco los valores.
En todo caso uno ve que cambia fuertemente la velocidad con el pH. Uno ve que el pH optimo de la pepsina esta cercano a pH 2, un poquito bajo a pH 2. El pH óptimo es el valor del pH, al cual la velocidad es máx., cuando se basa este estudio en función del pH.
Entonces uno ve que a ese pH acido, la tripsina cataliza la reacción, hay una alta densidad y a pH un poquito menos acido la velocidad baja, incluso a pH menos de 6, tipo 5,7, ya la velocidad prácticamente es 0; a pH 7 por ejemplo, según esta gráfica la velocidad es 0, no hay catálisis.
(alguien) ¿El pH óptimo, es cuando hay mayor velocidad? R: El pH para el cual la velocidad es mayor y eso es algo característico de la enzima. Cada enzima tiene un pH óptimo. ¿Por qué será que la pepsina tiene un pH óptimo tan re-bajo?, eso es algo muy especial, un pH tan bajo, ¿cuál será la razón fisiológica o como se quiera llamar? R: Resulta que el jugo gástrico justamente tiene un pH entre 1 y 2. Claro, tiene que poder catalizar la reacción en condiciones en las cuales esta.
Otro ejemplo, la glucosa-6-fosfatasa hepática.
Glucosa-6-fosfatasa hepática
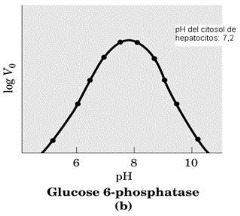 Aquí uno ve nuevamente que la velocidad cambia en función del pH, cambia fuertemente. Este tipo de curva, que se obtiene en un grafico de velocidad de reacción en función del pH, se llama curva acampanada.
Aquí uno ve nuevamente que la velocidad cambia en función del pH, cambia fuertemente. Este tipo de curva, que se obtiene en un grafico de velocidad de reacción en función del pH, se llama curva acampanada.Esto es lo típico, esta situación que aumenta, hay una zona de máxima que es relativamente ancho y después baja, o sea, la curva es acampanada.
Si uno hiciera aquí velocidad directamente, no logaritmo, tendría igual algo parecido.
Aquí la situación es totalmente diferente, el pH óptimo es cercano a 8, un poquito bajo 8. Y esto tiene relación con el pH del citosol de los hepatocitos que es 7,2; o sea, aquí el pH óptimo no es idéntico al pH de la enzima citosólica, al pH del entorno del microambiente en el cual normalmente esta la enzima en vivo, pero a lo menos parecido, no necesariamente tiene que ser idéntico.
Esto es el asunto del efecto del pH, que ustedes ven que es fuerte, un efecto fuerte. Si uno hubiera hecho el ensayo de actividad a pH 4, no encuentra actividad catalítica, o sea, tiene uno que fijarse qué valor tiene que usar. Ahora uno podría pensar, ¿a qué se debe este efecto del pH sobre la velocidad de reacción catalizada por una enzima?, ¿qué podría uno pensar?. Ustedes no pueden predecir exactamente ¿por qué el pH es 7,2?, ¿pero más o menos cuáles son los factores que hacen que el pH afecte?, ¿que creen ustedes, podrían generar estos cambios de velocidad cuando hay cambio de pH? R: El pH es diferente del pH fisiológico, durante el ensayo de actividad catalítica, la enzima se podría desnaturar (repite la resp. que dijo alguien). Probablemente, si uno pone esta glucosa-6-fosfatasa en un pH 4 y hace su ensayo de actividad catalítica a 30º, probablemente una parte se desnature; pero yo diría que a un pH cercano al pH optimo, no tendría porque denaturarse. Tan terrible no es eso de la inestabilidad de las proteínas, hay algo más relacionado de como cataliza la enzima.
¿Se acuerdan de algún mecanismo catalítico? Hay aá que se comportan como ácidos y bases débiles (repite resp. de alguien), ¿cuáles son esos?, ¿a qué se puede deber este efecto fuerte del pH sobre la velocidad de reacción catalizada por una enzima?, ¿pero algo más relacionado con el mecanismo de reacción? R: Hay aá que tienen grupos con características de acido débil y base débiles, eso es cierto!! ¿Cuál tipo de aá se comporta como acido y base débil? R: La lisina, se clasifica como aá básico, su cadena lateral tiene un grupo funcional amino, grupo base.
Supongamos que una enzima tiene muchas lisinas, pero de todas esas lisinas, ¿cuáles serán la que mas importan para la velocidad de reacción? R: Si hay una lisina en el sitio activo y no esta ahí solo casualmente como espectador, sino que es uno de los residuos que es llamado residuos catalíticos, que participan en el mecanismo de reacción. Entonces ahí es importante si en el mecanismo catalítico tiene que estar protonada la lisina, para ese protón entregárselo al sustrato en alguno de los pasos del mecanismo. Entonces se necesita un pH tal, de que este protonada a lo menos un buen porcentaje de toda la molécula de la enzima tenga esa lisina protonada. Entonces ahí hacia pH menos acídicos que el pH que al cual esta menos protonada, uno ahí va a disminuir la velocidad. Y al revés otros residuos puede uno pensar, que necesitan estar no protonados, porque tal vez en el curso del mecanismo de reacción aceptan protones. Existe eso, diferentes residuos que participan y uno tiene que estar protonado y el otro no protonada, entonces lo optimo es un pH en el cual se logra la situación optima en general. Y uno puede hacer estudios y determinar que tipo de residuos puede generar esta baja de velocidad en esta zona, entonces tiene que ser otro residuo el que genera este aumento, con diferentes residuos involucrados. Y ahí con el estudio del pH sobre la velocidad de reacción uno puede llegar a plantear, esto puede ser un residuo tal. El tipo estudio del pH es lo que se hace para postular mecanismos catalíticos.
Efecto de la Temperatura
· La velocidad de reacción aumenta con la temperatura.
En general, ¿cómo afecta la T en la velocidad de reacción? R: La T hace que la velocidad aumenta. ¿Esto por qué? R: Porque se mueven más rápido las moléculas (repite resp de alguien).
Y pensando en la energía de activación, se había planteado que hay una barrera entre el reactante y el producto, y esa barrera de energía, se cuantifica como energía de activación y la energía de activación es la que determina la velocidad de reacción. Eso de la velocidad de movimiento en el medio de las moléculas, en el solvente, eso no seria valido para una isomerización, porque si una misma molécula que se va isomerizar no necesita moverse para chocar con otras y reaccionar con otras; esa parte no tiene sentido.
El problema es que hay una energía de activación, entonces en un instante dado solamente las moléculas que tiene la energía de activación, esa alta energía, para alcanzar el estado de transición esa son las que reaccionan y a una T mayor el promedio de energía de la molécula es más alto. La molécula en general, tienen una energía promedio mayor y hay una cierta distribución de energía según una curva de kausel, hay una distribución de energía pero dentro de esa distribución las que tienen una alta energía van a ser mas, esa son las que van a poder reaccionar; esa es la causa por la cual la T aumenta la velocidad de reacción.
· Un aumento de 10 °C aproximadamente dobla la V.
Eso es en la T normales de 10 a 20, de 20 a 30, fácilmente. Esto se deriva de alguna ley de alguna ecuación, es un valor experimental que es bien útil. Aquí uno ve el efecto es bastante grande entre 20º y 30º, la velocidad mas o menos se dobla.
· A mayor temperatura aumenta la desnaturación.
Entonces uno hace eso con una enzima, mide a 10º encuentra una velocidad, a 20º mas o menos el doble y sigue aumentando la T .¿Qué le va a pasar a la proteína si se sigue aumentando la T? R: La proteína se desnatura.
· Los dos efectos se contraponen: a partir se cierta temperatura V baja con la temperatura.
Estos dos fenómenos siempre ocurren, hay dos efectos que se contraponen la desnaturación y el aumento de velocidad. Entonces a partir de cierta T la desnaturación va ser notoria, porque a baja T la desnaturación prácticamente no es notoria.
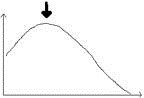 La desnaturación se presenta en lapsus de T relativamente estrechos ahí ya baja la T, entonces ahí baja la velocidad con la T y uno va a tener un sector en cual aumenta y después aumenta menos y después ahí baja, en un rango de T relativamente estrecho.
La desnaturación se presenta en lapsus de T relativamente estrechos ahí ya baja la T, entonces ahí baja la velocidad con la T y uno va a tener un sector en cual aumenta y después aumenta menos y después ahí baja, en un rango de T relativamente estrecho.Si uno hace un estudio para una enzima en particular con un ensayo de actividad catalitica, uno va encontrar algo así:
Hay una zona en la cual la velocidad aumenta, después aumenta menos en otras zonas y después baja.
· Las enzimas no presentan una “temperatura óptima”.
Si uno tiene este grafico, uno puede encontrar algún máximo en esta grafica, sin embargo, no existe para una enzima una T optima (uno podría pensar que dice máximo en el grafico); así como la enzima si tiene una un pH optimo. Una T óptima no existe para las enzimas. Porque resulta que… ¿a qué T uno encuentra ese máx..?, depende de cómo uno hace el ensayo de actividad catalítica. Si uno siempre usara exactamente el mismo ensayo, claro que va a encontrar el máx. en la misma parte, pero existen diferentes métodos de medidas de actividad catalítica. Lo que mas importante es durante cuanto tiempo uno mide, si esta encubando la enzima durante 10 minuto, este máx. se va a encontrar a una menor T, que si tal vez hace un ensayo en que mide durante dos días, en ese sentido las enzimas no presentan una T óptima.
Una enzima como cualquier proteína puede ser más o menos termoestable, hay proteínas más termoestables y se encuentra una correlación con su origen. Se espera que las proteína de un microorganismos marino del sur de chile sean bastantes no termoestables, porque vive a baja T., hay otras proteínas mucho mas termoestables.
Los Ensayos de Actividad Enzimática
· Se prepara un medio de reacción (contiene todo, menos la enzima)
Eso es la forma más clásica. ¿Qué le pondría al medio de reacción?, porque eso de todo no es muy preciso. R: Se le agrega un sustrato de la enzima Por ejemplo, para la exoquinasa, se le agrega glucosa (sustrato) y ATP. La exoquinasa cataliza la trasferencia del fosfato del ATP a la glucosa, se forma glucosa 6 fosfato y ATP. También se le agrega un tampón.
¿Qué tipo de tampón?, ¿qué características tiene que tener para que sirva?, hay tres características que definen un tampón. R: Un sistema tamponante HOAc/OAc-; en segundo lugar la concentración del tampón y tercer punto el pH del tampón, porque el HOAc/OAc- que tiene un pKa de 4,7 se puede preparar un tampón de pH de 4.5 o 4 .7, 4.8.
Entonces ¿con qué criterio se escoge el tampón que se va a usar? R: Uno usa un tampón que tenga un pH igual al pH óptimo de la enzima, para tener una alta velocidad. Y se usa una concentración adecuada, para que tenga una capacidad adecuada, o sea, que no cambie el pH durante la reacción, pero lo básico es el pH. Además la exoquinasa necesita cofactor Mg+2, entonces se le hecha por ejemplo sulfato de magnesio en concentración adecuada como para que la enzima este saturada de su cofactor.
Para que la reacción se inicie, se le agrega la enzima.
· Se tempera
· Se agrega la enzima
En un baño termorregulado se tempera a la T que va a usar en el ensayo. No hay T óptima, entonces lo normal que se usa es una T, por sobre la T ambiente. Uno necesita una T que se mantenga constante, en un baño termorregulado que calienta, porque los baños que enfrían son más caros y escasos. Lo típico es como 30°, para algunos ensayos es 35°, a gusto de la persona que lo monto. Entonces eso de temperar viene antes de agregar la enzima porque, resulta que ya tiene que estar a esa T constante, para tener sus condiciones estandarizadas, una vez que uno agrega la enzima la cuestión es muy rápida. A penas se agrega la enzima empieza la reacción.
· En un “ensayo de tiempo fijo” se para la reacción después de cierto tiempo (corto).
Significa que primero inicia la reacción agregando la enzima y después, se para la reacción después de un cierto tiempo que es relativamente corto, típico 5 minutos o 10 minutos, tal vez mas corto. Hay algunos casos excepcionales en los cuales la cuestión es de tal forma que los hacen en 20 minutos o mas largo.
¿Cómo uno logra parar la reacción? R: Se le puede agregar un inhibidor y si no hay un inhibidor adecuado, se agrega algo común, un poquito de acido fuerte. Es mas común un ácido que base fuerte o en algunos ensayos lo hacen en un tuvo eter, lo tiran en un baño de agua hirviendo o lo colocan en un baño de liquido. De alguna manera se logra detener la reacción, para un inhibidor es algo muy conveniente. Todo eso depende del ensayo que se monta.
· Se determina la [P]
Después de eso, se tiene que determinar cuánto producto se formó, lo típico es determinar la cantidad de producto, uno también podría determinar cuánto sustrato quedo. Lo mas típico en este tipo de ensayos, porque uno parte de productos prácticamente 0, no hay producto al inicio, a menos que sea una impureza. Entonces se determina la [P] por algún método químico.
· Se calculan los μmoles de P
· Se calculan el número de U y la concentración de la enzima en la muestra (U/ml).
Puede calcular lo micromoles del producto formado, ¿para qué serviría? R: Si uno quiere calcular unidades tiene que calcular cuántos micromoles se formaron, hay que tener en cuanta el volumen, y con el tiempo fijo que tenia, calcula la velocidad, y a partir de la velocidad puede calcular el número de unidades y la [E] en la muestra, unidades de muestra por ml dependiendo del volumen que agrego se calcula U/ml.
· Se puede calcular la actividad específica, A.E. (U/mg)
Además uno puede calcular la actividad específica, que son unidades por miligramo de proteína totales de la muestra.
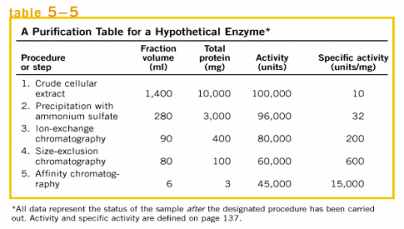
Tabla de Purificación de una Enzima Hipotética
· La actividad específica mide la pureza de la muestra de enzima
Por ejemplo, si uno purifica una enzima. Obviamente tiene que ir midiendo la actividad catalítica, para ver en que fracciones está la enzima.
Aquí tenemos los diferentes pasos del protocolo de purificación.
Después de cada paso que midieron el volumen de la solución; después de cada paso informa proteína totales, eso significa que con un poco de la solución del ensayo de proteínas, determinaron este dato de mg por ml, concentración de proteínas.
Con ese dato ¿qué más hicieron para llegar a la tabla?, o sea, tienen un cierto volumen de solución después de cada paso, entonces con esa solución para cada una de esas soluciones midieron mg de proteínas y ¿qué midieron, qué pusieron en la tabla en realidad?, si con el extracto puro encontraron que tiene 20 mg de proteína por ml, ¿cómo llegaron a este 10000 mg?, ¿cómo se llega a la proteína total, conociendo la concentración de proteínas y conociendo el volumen? (las proteínas siempre se miden en mg, no se pueden pasar a molaridad). R: Si uno tiene mg por ml, si multiplica por el volumen (ml), uno va obtener mg totales (mg/ml x ml= mg); eso es lo que pusieron en la tabla. Midieron concentración, multiplicaron con el volumen y pusieron mg totales.
Con la unidad, ¿qué es lo que midieron en el ensayo de actividad enzimática? R: Se mide velocidad de reacción en el ensayo y con esa velocidad de reacción, uno llega a unidades por ml (U/ml), [E] en la muestra que uso. Y esas unidades por ml con el volumen total que hay, uno pasa a unidades totales. Igual que con la proteína uno multiplica por el volumen y llega a la actividad total.
¿Cómo se genera esta tercera columna? R: Se dividen las unidades por los mg, se obtiene las unidades.










0 comentarios:
Publicar un comentario