La parte cinética es lo más representativo de la enzimología, tal vez lo más importante y también donde mas fácilmente uno se puede equivocar por problemas con los conceptos.
Hemos visto la parte general e introductoria, estructural, como modelos de sitios activos, pero esto es algo totalmente diferente.
Estudios Cinéticos: se mide la velocidad de la reacción catalizada
En una publicación se coloca que se obtuvieron “resultados cinéticos”, son estudios cinéticos. En este caso no tenemos ninguna información estructural, uno puede no tener idea si la enzima es una tetrámero, es un monómero o dónde se encuentra su sitio activo (por ejemplo), pero midió velocidades y obtiene resultados, mide la velocidad de la reacción catalizada.
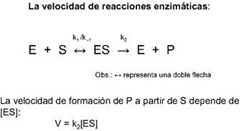
Recordando la parte cinética de la química general:
Si la reacción fuera A + A à B en la ecuación [A] se coloca al cuadrado porque es una reacción de 2do orden.
E = Enzima
ES= Complejo Sustrato- Enzima
P = Producto
En la velocidad de reacción catalizada por enzima participa la enzima, la enzima se une al sustrato y cuando están unidos es que ocurre la reacción.
Entonces hay que tomar en cuenta esta reacción: El S se une a la E en forma reversible, quiere decir que forma el ES y luego puede disociarse nuevamente.
- Hay una “k1” para el proceso de asociación (formación ES)
- “k-1” para el proceso de disociación ES
- k2 que es la constante de velocidad en la cual el S se transforma en P estando en sitio activo.
La velocidad de formación del producto que es lo que normalmente se mide cuando se quiere cuantificar la velocidad de reacción.
Entonces acá uno ve que el producto se formó a parte del complejo ES, entonces la velocidad de formación del producto tiene que depender de [ES] y de k2
¿De qué depende la [ES]?
R. Depende de la [S] y de [E].
Entonces uno ve de inmediato que para una reacción catalizada por una enzima la velocidad de reacción no va a depender solamente de la concentración de sustrato, [S], y punto.
Si la enzima necesita un cofactor y este no es de un grupo prostético significa que el cofactor se une reversiblemente a la enzima. Solamente las enzimas que tienen unido el cofactor van a tener actividad catalítica así es que la concentración del cofactor también es importante.
Si uno quiere hacer experimentos genéticos tiene que tener en cuenta todos estos factores para obtener resultados que sean significativos e interpretables para no cometer errores.
Velocidad inicial= Vo
Cuando uno mide la velocidad de una reacción catalizada por una enzima
Aà B (Catalizado por E)
Si uno grafica [B] v/s Tiempo entonces uno tiene un tubo de ensayo, le agregamos el reactante, (A), le agregamos la enzima, y comienza la reacción, pero la velocidad de reacción no se mantiene por mucho tiempo
Entonces si uno mide velocidad es importante hacerlo en un lapso de Tiempo adecuado, porque si uno hace delta P/ delta T para calcular pendiente no es lo correcto, porque esa pendiente ya no refleja velocidad inicial. Uno tiene medir velocidad en un lapso de tiempo tal que todavía se mantenga esa velocidad que sin dunda hay, un lapso de tiempo corto.
Entonces la velocidad no se mantiene por mucho tiempo, por una parte porque el reactante se está gastando y también por otros factores.
No se puede medir cuando se comienza la reacción porque hay un solo valor.
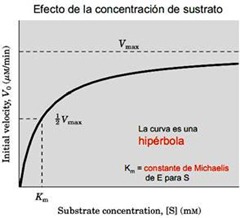 Acá se ve cómo la concentración de sustrato afecta la velocidad inicial, Vo, en concentración micromolar/minuto. Si uno en la ecuación no le coloca que es velocidad inicial es simplemente porque no siempre se escribe, pero está implícito, porque SIEMPRE es la velocidad inicial, no tendría sentido si la Vo no se incluyera.
Acá se ve cómo la concentración de sustrato afecta la velocidad inicial, Vo, en concentración micromolar/minuto. Si uno en la ecuación no le coloca que es velocidad inicial es simplemente porque no siempre se escribe, pero está implícito, porque SIEMPRE es la velocidad inicial, no tendría sentido si la Vo no se incluyera.Uno acá ve que aquí la Vo v/s [S] tiene un comportamiento curvo para bajar concentraciones de sustrato. A altas [S] se indica Velocidad Máxima (Vmáx).
Velocidad máxima es la asíntota a la curva.
Esta curva no es cualquier curva, se llama HIPÉRBOLA (igual que en la unión de oxígeno mioglobina).
Km es la constante de Michaelis y es de la enzima para el sustrato en cuestión y es ½ de la velocidad máxima exactamente.
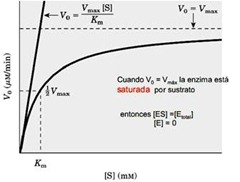 En esta curva se trató de ver hacia dónde tiende esta hipérbola, se extrapoló, esta sería la velocidad máxima a la cual tiende, de esto se intercepta en la mitad, se interpoló, y abajo obtenemos el valor del Km.
En esta curva se trató de ver hacia dónde tiende esta hipérbola, se extrapoló, esta sería la velocidad máxima a la cual tiende, de esto se intercepta en la mitad, se interpoló, y abajo obtenemos el valor del Km.Entonces esa recta es lo que uno espera si no fuera una reacción catalizada por una enzima, es decir una reacción química cualquiera donde S à P.
La hipérbola mostrada ilustra un comportamiento típico, hay reacciones catalizadas por enzimas que muestra un comportamiento atípico.
Michaelis y Menten hicieron esta ecuación basados en la hipérbola que demuestra el comportamiento de una reacción catalizada por enzimas.
Km= [S] a la cuál la velocidad de reacción es igual a ½ de la Vmáx.
Lo anteriormente dicho se puede deducir si en la ecuación anterior hacemos [S] = Km
Vo= (Vmáx)(Km)
2km
Los Km se simplifican y nos queda que
Vo= Vmáx
2
-
El sustrato no reacciona cuando no está unido al sitio activo de la enzima.
Ej. A bajas [S], cuando la [S] es mucho menor que Km, primero hay un aumento, es forma más o menos lineal, luego se curva y después la velocidad tiende a la velocidad máxima (asíntota).
¿Por qué siendo que se está aumentando la [reactante] que es el sustrato, no aumenta la velocidad de reacción y empieza a tener la forma asintótica?
Todas las moléculas de enzima ya tienen sustrato unido, entonces a partir del complejo enzima-sustrato se forma el producto y si ya no se puede formar más complejo, cuánto complejo ES puede haber es nuestro limitante y eso depende de cuanta enzima hay.
Teóricamente la velocidad máxima no se alcanza nunca, pero en la práctica si la concentración [S] es mucho mayor que Km se puede decir que es más o menos la velocidad máxima y eso se deduce de la ecuación:
 Si la [S] que es la variable, es mucho mayor que Km, imaginando que uno fuera mil y otro fuera uno, uno matemáticamente puede despreciar el término y simplifica el otro nos queda que la velocidad es igual a la velocidad máxima. Si lo vemos en forma precisa, realmente no es la velocidad máxima porque aquel Uno que colocamos realmente no es Cero, entonces depreciarlo siempre es una aproximación nada más.
Si la [S] que es la variable, es mucho mayor que Km, imaginando que uno fuera mil y otro fuera uno, uno matemáticamente puede despreciar el término y simplifica el otro nos queda que la velocidad es igual a la velocidad máxima. Si lo vemos en forma precisa, realmente no es la velocidad máxima porque aquel Uno que colocamos realmente no es Cero, entonces depreciarlo siempre es una aproximación nada más.*[S] muchos mayor que Km entonces la velocidad tiende a Vmáx, prácticamente no cambia la velocidad al agregarle sustrato. (Vo = Vmáx) ß reacción de orden cero.
Cuando se hace el experimento y se hace la hipérbola, todos los otros factores que afectan la velocidad hay que mantenerlos constante, entonces la [E] es constante.
Vo = Vmáx, se dice que la enzima está SATURADA por sustrato, porque ya está en forma de complejo ES y no es capaz de unirse con más sustrato para formar producto porque No queda enzima libre.
Pregunta en una prueba.
¿Qué pasa cuando una enzima está saturada?
R: La reacción procede con velocidad máxima.
Si hago otro experimento y uso la misma [S], pero le agrego el doble de enzima. Obtenemos también una hipérbola la cuál estaría sobre la otra y entonces la Vmáx va a ser el doble que en el experimento anterior, porque tendremos el doble de enzimas que se podrán complejar. El Km sería el mismo porque es una constante de la enzima para ese sustrato en particular.
Si la V es = ½ de la velocidad máxima y eso es porque [S] = Km ¿Qué pasa con estas concentraciones? La ½ de la E va a estar como complejo ES y la otra 1/2 va a estar como E libre.
¿Qué pasa si yo uso una [S] que es 50 veces el Km ([S]= 50Km)? ¿Qué fracción de la velocidad con respecto a la velocidad máxima tendré en esa situación?
Reemplazando:
Vo= (Vmáx) (50) entonces la velocidad es 98% de la velocidad máxima.
51
Uno también puede hacer la pregunta a la inversa, si yo quiero que la velocidad sea el 90% de la velocidad máxima ¿Cuál es la concentración de sustrato que necesito? (conociendo el Km)
Si uno quiere determinar el Km es algo interesante porque es una constante, Km de la enzima respecto a su sustrato y uno desea obtener el resultado experimentalmente.
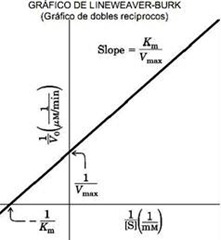
Uno tiene que tener constantes todos los factores, solamente variar [S], se obtiene una tabla de datos, se grafica y con la hipérbola no es muy fácil llegar al Km porque uno tiene que extrapolar la curva, entonces por la gráfica no es fácil extrapolar una curva, y no es lo óptimo, entonces en este caso ocupamos otra ecuación:
 Esta ecuación indica que si uno graficara 1/Vo en función de 1/[S] ¿Qué tipo de gráfico sería? R: Lineal, y su pendiente sería Km/Vmáx
Esta ecuación indica que si uno graficara 1/Vo en función de 1/[S] ¿Qué tipo de gráfico sería? R: Lineal, y su pendiente sería Km/VmáxSi 1/[S] es cero, entonces todo el término se hace cero y 1/Vo= 1/Vmáx.
Para que 1/[S] sea cero la [S] debe ser muy alta.
Entonces cuando se extrapola a concentración de sustrato infinita cuyo recíproco es cero.
Cuando 1/Vo=0 se tiene que 1/[S]=-1/Km
¿Cuál es la unidad de Km según su definición?
R: Concentración de sustrato (micromolar, milimolar, etc.)
Acá tenemos de forma gráfica la Vmáx y el Km. Generalmente el gráfico de recíprocos se usa aún en las publicaciones.
Ejemplos:
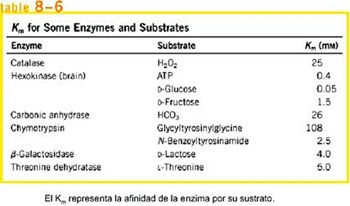
Catalasa: Cataliza la descomposición de agua oxigenada, entonces como sustrato tiene el peróxido de hidrogeno y el Km=25 mM
Los sustratos de la Hexoquinasa son ATP y D- glucosa. Hexo alude que la glucosa tiene 6 carbonos y quinasa a las enzimas que introducen grupos fosfatos.
Acá se ve que hay un km para cada sustrato y también en este caso se hizo un experimento donde se utilizó D- fructosa en vez de D-glucosa y se le encontró también su Km, es decir la Hexoquinasa no es completamente específica con respecto al azúcar, puede fosforilar también fructosa, pero sigue siendo su sustrato más importante la glucosa, eso se ve en el valor de km, donde es mucho menor la concentración para la glucosa que para la fructosa. Entonces, en Km representa la afinidad de la enzima por su sustrato.
Dijimos que la Vmáx depende de la [E] que se está usando, entonces la Vmáx no es una constante para la enzima como lo sería el km.
Qué tan rápida es en generar la transformación está representado por la constante catalítica
 Hay que imaginarse la situación: Hay una molécula de enzima y esta se une al sustrato, lo transforma en producto, llega otra molécula de enzima al sustrato, también la transforma en producto y así sucesivamente, pero la misma molécula de enzima, por eso se dice Número de Recambio, porque hay un recambio en el sitio activo. Entonces el número de recambio mide cuántas moléculas puede transformar a P esta única molécula de enzima por unidad de tiempo.
Hay que imaginarse la situación: Hay una molécula de enzima y esta se une al sustrato, lo transforma en producto, llega otra molécula de enzima al sustrato, también la transforma en producto y así sucesivamente, pero la misma molécula de enzima, por eso se dice Número de Recambio, porque hay un recambio en el sitio activo. Entonces el número de recambio mide cuántas moléculas puede transformar a P esta única molécula de enzima por unidad de tiempo. No hay falta de sustrato en este caso, siempre hay uno a la espera de ser transformado.
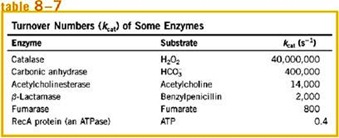
Acá nuevamente tenemos la catalasa con un número de recambio de 40 millones, quiere decir que 1 molécula de catalasa en 1 segundo transforma 40 millones de moléculas de H2O2.
Uno se imagina las situaciones que ahí aparecen, como por ejemplo [S] << Km y se va colocando los valores en las ecuaciones anteriores.
Finalmente nos da una constante, multiplicada por [E] y [S], en el fondo es como si uno tuviera una reacción bimolecular entre E y S.
Si uno tuviera por ejemplo una enzima y hay diferentes sustratos los cuales compiten por la misma enzima ¿Cuál de ellos gana imaginando la misma concentración de sustratos? R: El sustrato que tenga un Kcat/Km más alto, entonces medimos capacidad catalítica de la enzima y además refleja especificidad (más que el km solo).
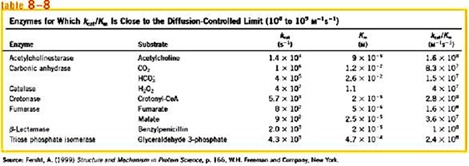
En todos los casos el Kcat/Km es cercano a lo que es el valor límite de un proceso controlado por difusión y eso es un valor entre 1x108 y 1x109 y su unidad es M-1s-1 ß M es molar y s es segundo.
Para una reacción bimolecular A+B àC V= K [A][B] entonces si la reacción es más rápida entonces la K de velocidad es más alta, sin embargo uno sabe que esta constante de velocidad tiene un límite superior, no puede ser mayor que 1x108 1x109, más o menos en este intervalo en unidad M-1s-1, porque es lo más rápido que puede difundir las moléculas en el solvente acuoso a esta T°.
Entonces todos los procesos que tengan una constante tan alta se dice que están limitados por difusión, es una reacción súper rápida, pero en lo que se demora es en que se difundan y se junten.














0 comentarios:
Publicar un comentario