La proteína la podemos polipeptidar por método clásico o método moderno que nos permita ver las cantidades de la proteína pura. Esta proteína una de las cosas importantes es determinarle su composición de aminoacídica, se hace hidrolizando la proteína completamente en 6M de HCl a 110 °C y en vacio para que no se destruyan los residuos de aminoácidos. Estos se separan por cromatografía de alta resolución. Por esa metodología podemos conocer la composición aminoacídica.
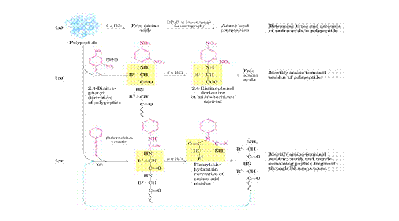
Otro aspecto importante es conocer el amino terminal, ya que nos va a definir cual es el péptido inicial (con que aminoácido comienza la secuencia) y eso se puede realizar con FDNB (2,4-dinitrofluorbenceno) que modifica específicamente el amino terminal, modifica otros grupos aminos pero se puede diferenciar fácilmente. Los aminoácidos de la épsilon-lisina por ejemplo, reaccionan con el FDNB pero tiene una característica totalmente distinta que se puede separar. La proteína se hidroliza y el aminoácido modificado en el amino terminal lo podemos identificar por cromatografía de capa fina.
Finalmente se obtiene una serie de cadenas polipeptídica tratándolas con proteasas y cada uno de estos péptidos se le puede determinar su secuencia por degradación de Edman, que es un método que actualmente esta absolutamente automatizado.
El carboxilo terminal se puede reconocer por una enzima específica que es capaz de ir sacando aminoácidos del extremo carboxilo terminal.
 Finalmente lo que uno tiene que realizar es que a partir de los péptidos (la secuencia de cada uno de los péptidos) reconstruir la secuencia correcta inicial.
Finalmente lo que uno tiene que realizar es que a partir de los péptidos (la secuencia de cada uno de los péptidos) reconstruir la secuencia correcta inicial.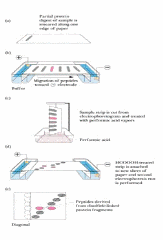 Hay un punto que es relevante conocer ¿dónde están ubicados los puentes disulfuro en una proteína? Se puede hacer de forma experimental. Con una de las enzimas que se utilizó para preparar los distintos péptidos, degradar la proteína, por lo cual se obtiene una mezcla de péptidos, antiguamente se hacia en papel, ahora hay otros soportes cromatográficos como capa fina, donde uno pone el hidrolizado de péptidos y los separa por cargas, acá están marcados los que tienen el azufre de un color rojizo, es solamente como referencial. Luego lo que se hace cuando se logra la separación, se trata la placa en un sentido con ácido perfórmico para romper los puentes disulfuros y por lo tanto si hay dos péptidos que estaban unidos por puente disulfuro ahora son dos péptidos distintos y al cambiar la polaridad y correrlos en el otro sentido de la placa todos los péptidos que no tenían puente disulfuro se agrupan en una diagonal y los que salen de la diagonal son péptidos que se lograron separar y estaban unidos por puente disulfuro por lo tanto se pueden tomar estos péptidos, secuenciarlos y ahora saber cuales péptidos están unidos por puentes disulfuros.
Hay un punto que es relevante conocer ¿dónde están ubicados los puentes disulfuro en una proteína? Se puede hacer de forma experimental. Con una de las enzimas que se utilizó para preparar los distintos péptidos, degradar la proteína, por lo cual se obtiene una mezcla de péptidos, antiguamente se hacia en papel, ahora hay otros soportes cromatográficos como capa fina, donde uno pone el hidrolizado de péptidos y los separa por cargas, acá están marcados los que tienen el azufre de un color rojizo, es solamente como referencial. Luego lo que se hace cuando se logra la separación, se trata la placa en un sentido con ácido perfórmico para romper los puentes disulfuros y por lo tanto si hay dos péptidos que estaban unidos por puente disulfuro ahora son dos péptidos distintos y al cambiar la polaridad y correrlos en el otro sentido de la placa todos los péptidos que no tenían puente disulfuro se agrupan en una diagonal y los que salen de la diagonal son péptidos que se lograron separar y estaban unidos por puente disulfuro por lo tanto se pueden tomar estos péptidos, secuenciarlos y ahora saber cuales péptidos están unidos por puentes disulfuros.¿Para qué sirve secuenciar una proteína?
Lo primero, de la secuencia vamos a poder obtener alguna idea de la funcionalidad que tiene esa proteína. Por ejemplo, proteínas de membrana tienen regiones hidrofóbicas, proteínas fibrosas tienen secuencias más atípicas. Podemos revisar con la secuencia de la proteína análisis de homología con otros organismos y ver por ejemplo cuán conservada es una proteína, incluso podemos hacer un árbol filogenéticos de las proteínas.
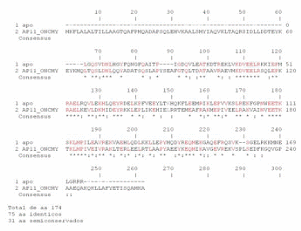 Aquí hay por ejemplo una comparación de una secuencia de la apolipoproteína A11 de “jarpa” con una apolipoproteína A11 “trucha arcoíris”, la comparación indica los residuos iguales con un asterisco y están en rojo, hay una con “dos puntitos” que corresponde a sustituciones conservativas. Hay dos tipos de sustituciones:
Aquí hay por ejemplo una comparación de una secuencia de la apolipoproteína A11 de “jarpa” con una apolipoproteína A11 “trucha arcoíris”, la comparación indica los residuos iguales con un asterisco y están en rojo, hay una con “dos puntitos” que corresponde a sustituciones conservativas. Hay dos tipos de sustituciones: - Conservativas: es cuando se conserva la característica del aminoácido, por ejemplo un básico con un básico.
- Semi-conservativas: Involucra otras cosas.
Esta es una comparación de distintas especies de la secuencia del citocromo C
¿Dónde esta ubicado el citocromo C?
En las mitocondrias, es uno de lo aceptores de protones de la cadena trasportadora de electrones, por lo tanto, es clave para la síntesis de ATP. Por consiguiente es altamente conservado en las especies que consumen oxigeno resultando ser una proteína clave.
 Ustedes pueden ver aquí que hacia abajo hay distintas secuencias que presentan variaciones en los aminoácidos, en cambio, los de color amarillo son los conservados 100%. Es otra manera de representarlo.
Ustedes pueden ver aquí que hacia abajo hay distintas secuencias que presentan variaciones en los aminoácidos, en cambio, los de color amarillo son los conservados 100%. Es otra manera de representarlo.¿Qué información se puede sacar? ¿Qué zonas de la proteína serian las más importantes?
Los más conservados (color amarillo)
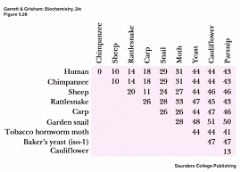 En caso de una mutación de uno de estos aminoácidos claves lo más probable es que el citocromo C pierda su función, el organismo no va a poder usar oxigeno para poder producir energía.
En caso de una mutación de uno de estos aminoácidos claves lo más probable es que el citocromo C pierda su función, el organismo no va a poder usar oxigeno para poder producir energía.En esta tabla esta puesta la diferencia en número de aminoácidos en el citocromo C. Entre los humanos y los monos no hay diferencia, entre humanos y ovejas hay 10 aminoácidos distintos, etc.
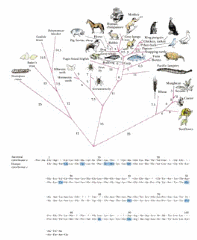
Filogenia del Citocromo C
· El numero de aminoácidos diferentes entre dos secuencias de citocromo C es proporcional a las direncias filogenéticas entre las especies de las cuales ellos derivan.
· Estas observaciones pueden ser usadas para construir árboles filogenéticos de proteínas.
· Éstas son las bases para los estudios de la evolución molecular
Este es un árbol filogenético, realizado desde la estructura del citocromo C, donde esta la relación con la diferencia de aminoácidos que se observan para clasificar los distintos animales.
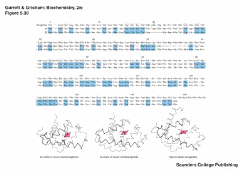
Otra cosa importante, aquí hace referencia a la hemoglobina, es que hay zonas que son claves en la proteína, están recalcadas de color azul. Por ejemplo aquí tenemos la hemoglobina se demuestra que con sus cadenas α y β son parientes de mioglobina y esto por secuencia primaria puede demostrarlo, más aún cuando uno llega a niveles de estructura se da cuenta que son proteínas muy relacionadas.
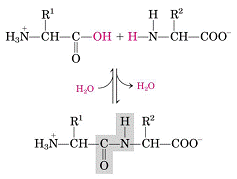
Para entender la estructura de la proteína lo primero que hay que entender es cómo se asocian los distintos aminoácido, estos aminoácidos para formar el polímero que es la proteína forman enlaces peptídicos y es una reacción entre el carboxilo terminal y el grupo amino terminal del aminoácido que le sigue, con perdida de una molécula de agua.
Cuando los aminoácidos están formando en este caso un dipéptido, hablamos de un residuo de aminoácido ya que han perdido a lo menos una molécula de agua. Este enlace peptídico determina una gran variedad de las características estructurales de la proteína porque tiene ciertas propiedades que las vamos a ver a continuación.
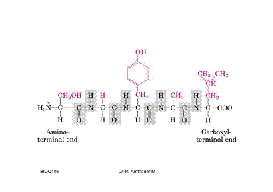
Cuando tenemos varios aminoácidos unidos, ya formamos un péptido. Por convención se denomina amino terminal donde empieza la proteína y carboxilo terminal donde termina. Esto es coincidente a como se sintetizan las proteínas en la célula el grupo amino terminal es el primer aá que se incorpora a la proteína y el grupo carboxilo es el ultimo que se incorpora. En rojo están los residuos R para los distintos tipos de aá que componen este péptido.
¿Qué característica tiene el enlace peptídico?
Por la naturaleza los átomos que lo componen y su característica la electronegatividad del oxigeno y el balance con la electronegatividad del hidrogeno, los electrones se distribuyen y por lo tanto es un enlace que tiene características parciales de doble enlace en realidad. Esto rigidiza los átomos que están formando el enlace peptídico.
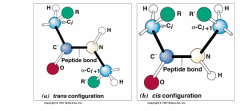 Este es el enlace peptídico, como mencionamos anteriormente tiene características parciales de doble enlace, al tener esta característica se puede formar con el resto de los átomos en una configuración cis o trans, por supuesto energéticamente la probabilidad esta desplazada hacia la configuración trans por los impedimentos estéricos, la probabilidad de encontrar configuración cis va a depender de los grupos R.
Este es el enlace peptídico, como mencionamos anteriormente tiene características parciales de doble enlace, al tener esta característica se puede formar con el resto de los átomos en una configuración cis o trans, por supuesto energéticamente la probabilidad esta desplazada hacia la configuración trans por los impedimentos estéricos, la probabilidad de encontrar configuración cis va a depender de los grupos R.Aquí hay algo importante, los átomos que están formando parte del enlace peptídico, dada la naturaleza que ya describimos que tiene, están en un mismo plano (coplanares). Por lo tanto las rotaciones que se producen en este ángulo que se denomina Ci entre el amino y el carbono-α del aminoácido. Y eso nos va a dar ciertas probabilidades de estructura.
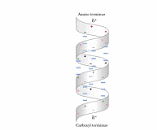
La α-hélice que forman los aminoácidos tiene característica particulares, donde comienza, abajo, quedan cargas negativas y donde termina, arriba, queda con carga positiva, o sea, se genera un pequeño dipolo que presenta carga y en el centro, estas cargas, están neutralizadas como vamos a ver por puentes de hidrogeno.
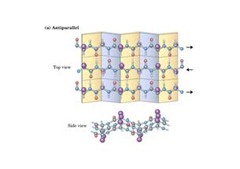
El otro elemento de estructura secundaria característico que esta en todas las proteínas presente: la hoja β plegada.
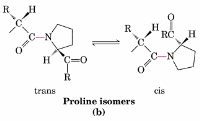
La prolina por ser un iminoácido tiene restringida la movilidad del amino, no es capaz entonces de formar ni α-hélice ni hoja β plegada.
Acá esta la prolina, puede estar en trans o en cis y por eso forma una vuelta muy cerrada porque el grupo amino esta formando parte del grupo R al mismo tiempo, lo cual rigidiza mucho la interacción entre los aminoácidos.
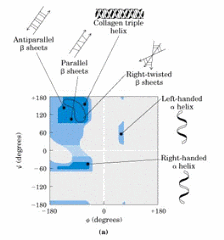
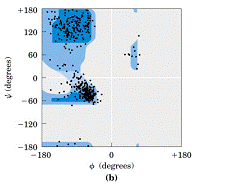
Aquí esta la explicación: de los planos entre dos enlaces peptídicos consecutivos, los distintos valores tienen no pueden ser cualquiera. Las zonas azules corresponden a las zonas energéticas favorables que pueden tomar. Y eso determina que tipo de estructura secundaria se van a formar.
Aquí están puestos los puntos las proteínas existentes con las estructuras y son muy pocas las que se escapan a lo que predice energéticamente la ecuación. Los puntos negros es la realidad de lo que se encuentra.
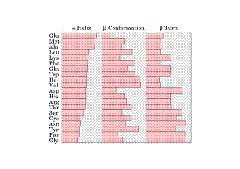 Lo que indica la barra es la probabilidad de encontrar un determinado aminoácido o la probabilidad del aminoácido de estar formando parte de una α-hélice, hoja β plegada o en una “vuelta en βeta” (vuelta cerrada).
Lo que indica la barra es la probabilidad de encontrar un determinado aminoácido o la probabilidad del aminoácido de estar formando parte de una α-hélice, hoja β plegada o en una “vuelta en βeta” (vuelta cerrada).En las α-hélice todos los aminoácidos quedan mirando hacia la periferia siendo muy estable de esta forma.
La mioglobina es una proteína formada sólo por α-hélice.
La mayoría de las estructuras primarias tienden a plegarse formando una estructura secundaria, puede ser α-hélice, hoja β plegada o en una “vuelta en β”, pero también hay zonas que no tienen estructura, eso es una “estructura al azar”. Estas estructuras secundarias participan en la formación de la estructura terciaria de proteínas globulares, pero hay proteínas como las fibrilares que, en general, se quedan en estructura secundaria. Por ejemplo las α-hélice forman las α-queratinas del pelo, de las plumas y de las uñas, que aparte de estar estabilizadas por puentes de hidrógenos, posee entremedio, entre α-hélice, puentes disulfuro, por lo tanto, forma proteínas que tienen una estructura muy robusta y que tienen distintos grados de dureza a su vez tienen distinto grado de flexibilidad.
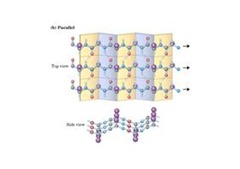
Propiedades de proteínas fibrosas: tienen estructuras muy alargadas y tienen conformación en hoja β, su característica principal es que son muy suaves y flexibles, por ejemplo la fibroína de la seda.
Finalmente un caso particular el colágeno es una estructura bien especial porque es una estructura de triple hélice, forma estructuras que son muy firmes pero que no tienen elasticidad y por lo tanto forman los tendones y la matriz de los huesos.
La queratina forma α-hélice y dos de estas α-hélice se sobre-enrollan sobre si mismas y se van ordenando para formar lo que se denomina protofilamentos, una detrás de la otra, y forman una hebra de 20 a 30Ǻ para luego formar una protofibrilla de 40 a 50Ǻ. Esta protofibrilla se asocia con el resto para formar los filamentos intermedios propiamente tal, que están dentro de la célula.










0 comentarios:
Publicar un comentario