Descripción de las Proteínas:
Estructural: las proteínas son el principal material de construcción de los seres vivos, formando pared de casi todas las estructuras: desde las membranas celulares hasta ser el principal constituyente del tejido conectivo (colágeno), del pelo y uñas (queratina), etc.
Almacén de aminoácidos: Algunas proteínas constituyen una fuente de reserva de aminoácidos (no de energía), lo que permite la síntesis de proteínas fundamentales durante los procesos embrionarios. Son abundantes, por tanto, en las semillas vegetales, en los huevos de los animales (ovoalbúmina de la clara de huevo) y la caseína en la leche de los mamíferos. El cuerpo humano no sintetiza los 20 aminoácidos, por lo que necesitamos de varios de ellos, los que implementamos por medio de la dieta.
No son fuente de energía pero como último recurso si son fuente de energía. El cual causa serios trastornos metabólicos en el organismo.
Transporte: Hay una gran cantidad de proteínas que pueden unir reversiblemente sustituyentes como la hemoglobina transporta oxígeno, albúmina transportador de ligandos (importante en farmacia), HDL, Mioglobina, Transferrina.
Catalizadores: Casi todas las enzimas son proteínas (hay también ribosimas que son RNA’s con actividad catalítica), actúan como catalizadores de las reacciones de los seres vivos.
Contráctil: Proteínas del huso mitótico, el movimiento es producido por la Tubulina.
Defensa y Protección: Sistemas de Inmunidad Adquirido e Innato, en el ámbito innato, hay un gran campo de investigación, las defensas básicas que tenemos desde que nacemos, tenemos proteínas con acción directa en la actividad bacteriana, por ejemplo la melitina, péptido producido por las avejas que está en el veneno de las avejas y en ciertos niveles en la miel.
Regulación del pH: Las proteínas contienen grupos que se conforma de ácidos débiles y bases débiles que pueden protonarse o desprotonarse a pKa’s cercanos al pH Fisiológico, participando en la regulación del pH.
Otros: Son proteínas, Tela de Araña, Seda. Las luciérnagas producen luz por medio de una reacción catalítica (función de proteínas), glóbulos rojos llenos de hemoglobina que le da el color rojo característico cuando está como óxido de hemoglobina combinado con el oxígeno, estructuras como los cuernos del rinoceronte son proteínas (son pelos).
Un péptido es un polímero de aminoácidos pequeños que depende del número de aminoácidos que lo están formando, como proteína se toma como un número de residuos sobre 100, bajo 100 hablamos de péptidos, es decir, bajo un peso molecular de 10000 hablamos de péptidos.
Tenemos una gran variedad a cuanto las características de las proteínas, son polímeros complejos.
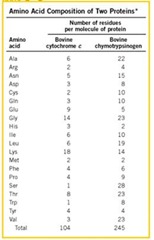
Si sabemos la composición de aminoácidos de una proteína, podemos deducir características ácido-base, solubilidad, etc. Desde el punto de vista nutricional es muy importante saber la composición de las proteínas, así sabemos que tan beneficiosas son las proteínas para la dieta.
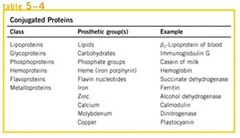 La mayoría de las proteínas poseen una estructura conjugada compleja, ya que no sólo poseen aminoácidos sino que también poseen otros grupos químicos unidos (enlaces covalentes o enlaces débiles).
La mayoría de las proteínas poseen una estructura conjugada compleja, ya que no sólo poseen aminoácidos sino que también poseen otros grupos químicos unidos (enlaces covalentes o enlaces débiles).La mayoría de las proteínas de membrana son Glicoproteínas.
El zinc ayuda a eliminar el alcohol, molibdeno importante para la fijación del nitrógeno en vegetales.
Desde el punto de vista de la arquitectura de la proteína se clasifican principalmente en 2 tipos:
Proteínas Globulares: Tiende a tener forma de pelota
Proteínas Fibrosas: La proteína forma una fibra larga.
Cualquiera de las 2 formas posee distintos tipos de estructura.
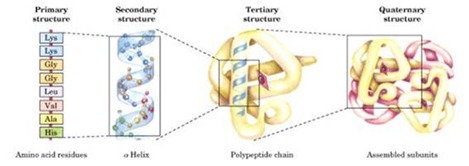
Primaria: Secuencia de aminoácidos
Secundaria: Estructuras locales estabilizadas por puentes de hidrógeno.
Terciaria: Estructura tridimensional de estas proteínas.
Cuaternaria: Organización en subunidades, varias cadenas polipeptídicas se unen para formar la proteína que funcionalmente es activa o que tiene funcionalidad biológica.
Todas las Proteínas presentan estructura Primaria, Secundaria y Terciaria.
En términos generales, para que las proteínas posean actividad biológica deben poseer estructura terciaria o cuaternaria.
¿Cómo podemos dilucidar la estructura de una proteína?
Para ello primeros tenemos que aislar la proteína (purificar) y para aislar la proteína nos deberemos fijar en los niveles de estructura, lo más importante es dilucidar la estructura primaria, a partir de esta podemos deducir la estructura secundaria y terciaria por medio de programas computacionales y dentro de estas estructuras ver qué elementos coinciden con ciertas funciones de las proteínas, por lo tanto podemos hacer una predicción sin saber toda la biología de la proteína, simplemente conociendo la estructura primaria.
¿Cómo se purifican las proteínas?
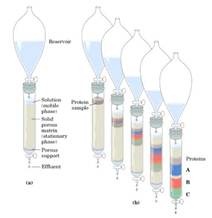
Una de las técnicas más utilizadas es la Cromatografía (forman patrones de colores distintos), permite separar compuestos gracias a la fase móvil y a la fase estacionaria. Entonces hay compuestos que pueden tener mas afinidad por la fase móvil, por lo tanto un compuesto se mueve mas rápidamente hacia esa fase y el otro a la fase estacionaria por lo tanto tiende a no moverse tanto.
Principios fisicoquímicos utilizados para separar proteínas:
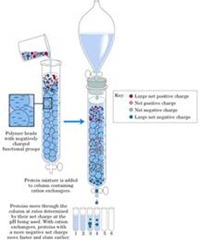
La fase estacionaria tenga carga negativa, así todas las proteínas que yo agregue a un pH determinado y que tengan cargas positivas quedarán retenidas en la matriz, se pasa el buffer y las negativas pasaran de largo; las positivas las puedo ir eluyendo de acuerdo a su carga, las que tienen poca carga positiva se retienen con menos fuerza que las que tienen una gran carga positiva y por lo tanto se pueden separar según las que no tienen carga, poca carga y alta carga positiva.
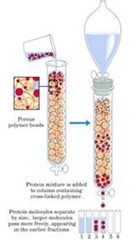
Separación según el tamaño (Cromatografía de Filtración) que en términos cromatográficos es una Cromatografía de Partición, ocurre por medio del material poroso que posee una fase liquida dentro de su poro y que está inmersa en la fase líquida que está fuera del poro. Entonces las moléculas muy grandes no se pueden particionar al interior del poro, en cambio, las más pequeñas si se particionan, entonces a medida que avanzan las moléculas las grandes salen primero y las más pequeñas se retardan más pudiendo separar así por tamaño.
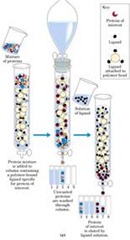
Una de las herramientas más poderosas es la cromatografía de afinidad, esta posee una fase estacionaria compuesta por una resina al que se le pone un ligando; por ejemplo si deseo purificar el receptor de la hormona de crecimiento, entonces debemos poner la hormona en la resina, en otras palabras uno la hormona de crecimiento a la fase sólida y por lo tanto de todas las proteínas que yo agrego (siempre que esté soluble el receptor para hormona de crecimiento), se va a unir a su ligando ( a la hormona) y va a quedar determinado y por lo tanto, al lavar la columna van a pasar todas las proteínas que no se unen y luego si yo agrego una gran cantidad de hormona de crecimiento voy a reemplazar la proteína unida y va a salir el receptor puro. Aunque en la realidad no es tan fácil purificar por cromatografía por afinidad.
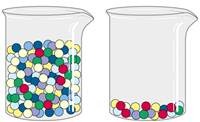 En la práctica se debe tener lo suficientemente purificada mi proteína antes de aplicar este método, también se sabe que nunca una matriz ha de ser lo suficientemente inerte y siempre hay alguna proteína que tiene algún tipo de afinidad extra por lo que hay interferencias en mi resultado.
En la práctica se debe tener lo suficientemente purificada mi proteína antes de aplicar este método, también se sabe que nunca una matriz ha de ser lo suficientemente inerte y siempre hay alguna proteína que tiene algún tipo de afinidad extra por lo que hay interferencias en mi resultado.Los colores de las esferas representan las distintas proteínas presentes en una solución que se encuentran solubles en un vaso. Se desean purificar las proteínas rojas, para ello se utiliza un método que enriquezca las esferas rojas y elimine las de otro color, esto es extremadamente difícil de realizar, aunque actualmente existen muchos métodos para poder llegar a obtener esferas rojas. Mientras más abundantes sea la proteína, más fácil es de purificar.
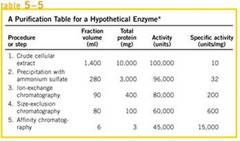 Para purificar por ejemplo una enzima debemos controlar las distintas etapas, una enzima es fácil de purificar ya que se puede monitorear en cada etapa. Se hace un extracto celular que tiene un volumen determinado, se cuantifica la cantidad de proteínas que se posee y luego se mide la actividad enzimática de mi enzima a analizar.
Para purificar por ejemplo una enzima debemos controlar las distintas etapas, una enzima es fácil de purificar ya que se puede monitorear en cada etapa. Se hace un extracto celular que tiene un volumen determinado, se cuantifica la cantidad de proteínas que se posee y luego se mide la actividad enzimática de mi enzima a analizar.1. Partimos de un extracto que posee 14000 ml 10000 mg de proteínas y una actividad de 100000. Si divido la actividad enzimática expresada en unidades partido por las proteínas esto es igual a 10 (actividad específica)
2. Luego se precipita con NH4SO4, bajo distintas condiciones, logro enriquecer mi extracto obteniendo 280 ml, 3000 mg de proteínas y una actividad de 96000. Lo importante es que sube la actividad específica, se disminuyó en 7 gramos la cantidad total de proteína, y mi actividad específica se triplicó, por lo que tengo 3 veces más pura mi proteína.
Luego aplicamos las Cromatografías:
Intercambio Iónico, logro aumentar a 200 actividad específica, Cromatografía de Exclusión (Filtración) 600 y ahora que está mi proteína mucho más purificada aplico Cromatografía de Afinidad luego de haber bajado de 10000 a 100 la cantidad de proteínas totales que tenía, se logra purificar 3 mg con una actividad de 15000 (purificación de 1500 veces). Cuando uno tiene sobre 1000 veces purificada su proteína se considera como que la proteína está prácticamente pura.
Existen muchas otras técnicas de purificación.
¿Cómo se chuequea si tengo pura mi enzima?
Por medio de otra técnica denominada electroforesis
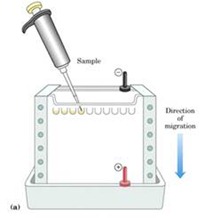
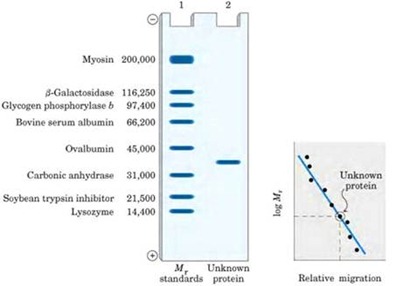
Es un gel de acrilamida que permite separar por tamaños moleculares las proteínas, por medio de corriente eléctrica, luego de separadas las proteínas, se tiñen con un colorante específico que se une a las proteínas de donde se obtienen patrones
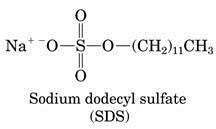
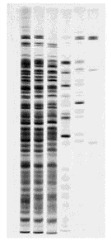 Muestra compleja que a medida que se va purificando el número de bandas disminuye. Una proteína no siempre muestra una sola banda, porque si la proteína está formada de varias cadenas polipeptídicas se verán varias cadenas polipeptídicas en la muestra, pero se puede tener una sola, esto sucede porque las proteínas en la electroforesis se separan utilizando por medio de un denaturante que es un detergente (Sodio Dodecil Sulfato)
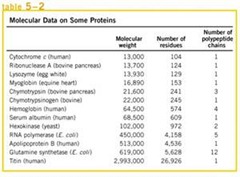
Muestra compleja que a medida que se va purificando el número de bandas disminuye. Una proteína no siempre muestra una sola banda, porque si la proteína está formada de varias cadenas polipeptídicas se verán varias cadenas polipeptídicas en la muestra, pero se puede tener una sola, esto sucede porque las proteínas en la electroforesis se separan utilizando por medio de un denaturante que es un detergente (Sodio Dodecil Sulfato)La electroforesis además sirve para conocer el peso molecular de la cadena polipeptídica que estamos analizando. Para ello hacemos reaccionar nuestra proteína desconocida con distintas proteínas a las que les conocemos el peso molecular, según la movilidad electroforética, por medio del log M (logaritmo del peso molecular) vs la Movilidad (cm.) es una recta calculamos los centímetros que se movió la proteína y con ello calcular el peso molecular.
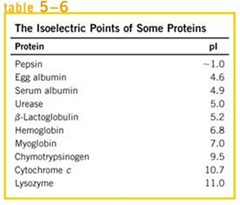 Todas las proteínas están conformadas por aminoácidos, por lo que otra característica que podemos determinar es su punto isoeléctrico. Al agregarle un gradiente de pH a mi electroforesis, la proteína sólo se va a mover hasta que alcance su punto isoeléctrico, y de esta manera podemos calcular el punto isoeléctrico.
Todas las proteínas están conformadas por aminoácidos, por lo que otra característica que podemos determinar es su punto isoeléctrico. Al agregarle un gradiente de pH a mi electroforesis, la proteína sólo se va a mover hasta que alcance su punto isoeléctrico, y de esta manera podemos calcular el punto isoeléctrico.Si tengo por ejemplo una proteína con un punto isoeléctrico básico, sin saber su cadena polipeptídica podemos deducir que presenta una gran concentración de aminoácidos básicos en su estructura primaria.
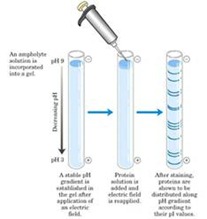 Para encontrar el PI también se prepara un gel de poliacrilamida y se le agrega una solución llamada anfolito (serie de compuestos cargados que al ser sometidos a un campo eléctrico generan un gradiente de pH estable. Por lo tanto cuando agrego proteínas y sigo agregando corriente, la proteína va a migrar por su carga, pero cuando alcanza su PI (carga 0) la proteína no se mueve más, y con ello calculamos el PI.
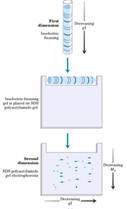
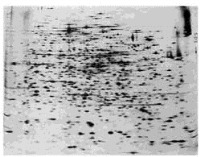
Para encontrar el PI también se prepara un gel de poliacrilamida y se le agrega una solución llamada anfolito (serie de compuestos cargados que al ser sometidos a un campo eléctrico generan un gradiente de pH estable. Por lo tanto cuando agrego proteínas y sigo agregando corriente, la proteína va a migrar por su carga, pero cuando alcanza su PI (carga 0) la proteína no se mueve más, y con ello calculamos el PI.Otra técnica sumamente efectiva, tomo un extracto de proteínas solubles y lo separo primero por su PI y luego ese gel lo tomo y lo pongo recostado sobre el gel de poliacrilamida y SDS (denatura proteínas) se obtiene una separación de proteínas formando un mapa (Electroforesis de 2 Dimensiones), 2 dimensiones porque he separado por dos propiedades fisicoquímicas (PI y por PM), obteniéndose manchas. Cada mancha es una proteína pura.
Esto es muy útil desde el punto de vista clínico, ya que para ciertas patologías cambia el número de proteínas que tenemos en la sangre (aparecen y desaparecen proteínas).
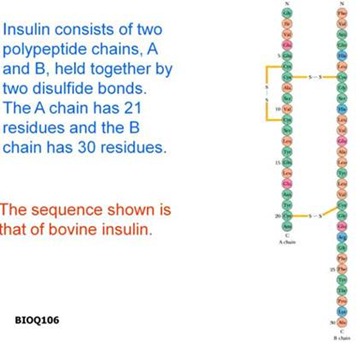
Cuando uno tiene la proteína 100% pura, lo que uno desea es llegar a determinar la frecuencia primaria, esto es mucho más complejo porque las proteínas presentan enlaces covalentes intercadenas, puentes disulfuro, puentes de hidrógeno y por lo tanto esto dificulta para determinar la frecuencia. Otra cosa que complica es cuando hay 2 cadenas unidas por puentes disulfuro, en este caso se debe romper el puente disulfuro y separar las 2 cadenas polipeptídicas y así poder hacer la determinación de la estructura primaria.
Determinación de la secuencia (8 pasos):
Si la cadena polipeptídica tiene más de una cadena hay que separarla.
Si tiene puentes disulfuro hay que reducirla (cortar enlace).
Determinar la composición de aminoácidos de cada cadena.
Determinar qué aminoácido está en el extremo amino terminal de la proteína y en el extremo carboxilo terminal.
Cortar cada cadena polipeptídica en fragmentos más pequeños para poder determinar la secuencia de la cadena completa
Repetir el punto anterior usando diferentes procedimientos para cortar la cadena y generar diferentes fragmentos
Reconstruir la secuencia de la proteína de las secuencias de los distintos péptidos que se generaron, esto se hace por sobreposición de los fragmentos
Determinar la posición de los puentes disulfuros.
Paso I: Separación de las Cadenas.
Dependen de fuerzas débiles
Separación se puede lograr por cambios de pH extremo (sobretodo en estructuras cuaternarias), 8M urea (rompe estructura secundaria de la proteína), 6M Clorhidrato de Guanidina, Alta concentración de Sal.
Paso II: Rompimiento de Puentes Disulfuros:
Oxidación con ácido perfórmico
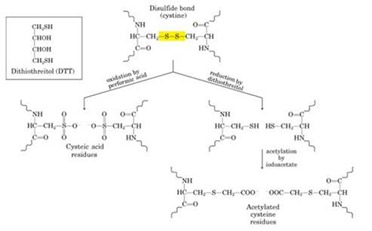 Agentes reductores del grupo sulfhidrilo (Beta-Mercaptoetanol, Ditiotreitol y para prevenir que se vuelvan a formar se utiliza un agente alquilante como el ácido yodoacético.
Agentes reductores del grupo sulfhidrilo (Beta-Mercaptoetanol, Ditiotreitol y para prevenir que se vuelvan a formar se utiliza un agente alquilante como el ácido yodoacético.Paso III: Determinar la Composición de Aminoácidos:
Disminuir la cantidad de fragmentos demasiados pequeños que se pueden formar, para que no sea tan tedioso luego armar el rompecabezas.
Paso IV: Identificación del extremo Amino y Carboxilo terminal:
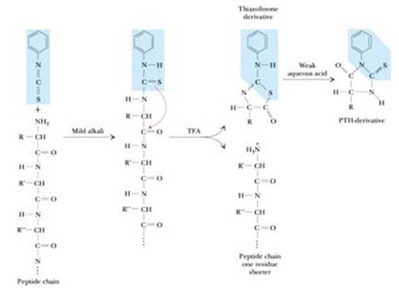
N-terminal: Por medio de un análisis con reactivo de Edman, fenilisotiocianato y derivados del mismo (derivados reaccionan con el grupo amino terminal de la proteína y después se corta con un ácido como el Trifluoracético y genera un derivado del primer aminoácido que se denomina PTH derivado que posee la característica de ser fluorescente).
C-terminal: Se puede hacer por análisis enzimático (carboxipeptidasa) que corre las proteínas por el lado C-terminal (saca aminoácidos por el extremo C-terminal). La Carboxipeptidasa A corta en cualquier residuo excepto si la proteína termina en prolina, arginina y lisina, mientras que la Carboxipeptidasa B, trabaja sólo con Arginina y Lisina.
Paso V y VI: Fragmentación de las Cadenas
Fragmentación Enzimática, se utilizan enzimas proteolíticas como tripsina, quimotripsina, clostripaína, proteasa del estafilococo, papaína, bromelina.
Fragmentación Química, se utiliza bromuro de cianógeno (extremadamente tóxico)
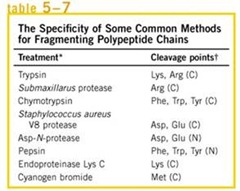
Fragmentación enzimática:
· Tripsina corta en el carboxilo terminal de lisina y Arginina
· Quimotripsina, corta en el carboxilo terminal de Fenilalanina, Tirosina y Triptófano
· Clostripaina, como Tripsina pero ataca a Arginina más que Lisina.
· Proteasa de Staphylococco
o Carboxilo terminal de Glutamina y Asparragina en buffer fosfato
o Específicamente para Glicina en buffer acetato o bicarbonato
Tripsina reconoce el lado carboxilo terminal de la Arginina y corta en este sector.
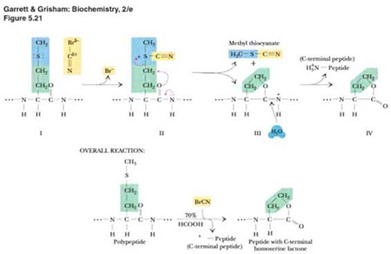
Fragmentación química:
· Bromuro de cianógeno (CNBr) actúa solo en residuos de Metionina
· CNBr es usado porque las proteínas usualmente tienen solo unos pocos residuos de Metionina.
· Se reconoce por un péptido en el carbono terminal, Homoserina lactona
Separación peptídica por HPLC
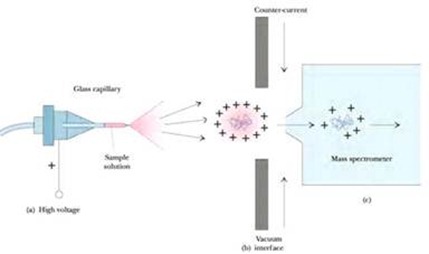
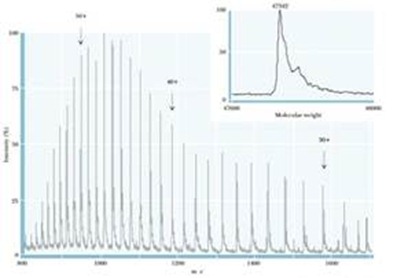
Secuenciación de los péptidos (espectrometría de masa)
Inmovilizamos el péptido en una región del instrumento. Hay un destello láser que fragmenta o suelta la muestra y la carga (está en vacío); hay un tiempo de vuelo que es tiempo que se demora hasta llegar a un detector y este tiempo de vuelo es dependiente de la masa.
Paso VII: Reconstrucción de la Cadena
Se utilizan 2 métodos por reacción de Edman o por Espectrometría de Masa (procedimiento más caro, que igual posee sus limitaciones, debido al algoritmo matemático “residuos sobre 30”)
Comparar corte por tripsina y proteasa de staphylococco en un péptido típico:
• Corte por Tripsina :
A-E-F-S-G-I-T-P-K L-V-G-K
• Proteasa de Staphylococcus:
F-S-G-I-T-P-K L-V-G-K-A-E
L-V-G-K A-E-F-S-G-I-T-P-K L-V-G-K-A-E F-S-G-I-T-P-K
• Secuencia Correcta:
L-V-G-K-A-E-F-S-G-I-T-P-K












0 comentarios:
Publicar un comentario