El agua está formada por un átomo de oxígeno, que es más grande que los de hidrógenos, tienen enlaces covalentes que unen el átomo de oxigeno a los átomos de hidrógeno, y en la última capa de electrones del oxígeno hay más electrones que no formaron enlaces y que están en orbitales, todo formando una estructura tetraédrica.
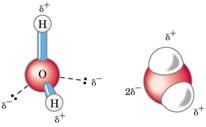
La molécula de agua hacia un lado tiene una carga parcial negativa que corresponden a estos electrones no enlazantes del oxígenos y hacia el otro lado los dos protones (H) están con carga parcial + se anota con la letra delta (δ).
 El agua líquida está formando puentes de hidrógeno con otros compuestos. Las moléculas de agua en el hielo forman una red cristalina perfectamente ordenada. El máximo de enlaces puente hidrógeno para una molécula de agua es de 4, aunque nunca se tienen los 4 enlaces. El agua posee una zona parcialmente positiva, que la proporciona el hidrógeno, y otra parcialmente negativa, que la da el oxígeno. El enlace hidrógeno es un enlace de relativa baja energía por lo tanto se están formando constantemente pero también se están rompiendo.
El agua líquida está formando puentes de hidrógeno con otros compuestos. Las moléculas de agua en el hielo forman una red cristalina perfectamente ordenada. El máximo de enlaces puente hidrógeno para una molécula de agua es de 4, aunque nunca se tienen los 4 enlaces. El agua posee una zona parcialmente positiva, que la proporciona el hidrógeno, y otra parcialmente negativa, que la da el oxígeno. El enlace hidrógeno es un enlace de relativa baja energía por lo tanto se están formando constantemente pero también se están rompiendo. No solo el agua forma puentes de hidrógeno, sino que cualquier grupo funcional que tenga un grupo OH- puede formar puentes de hidrógeno, ya que el hidrógeno en esas moléculas, en esos grupos funcionales, van a tener una carga formal positiva y se necesita un receptor de hidrógeno que es otro grupo funcional.
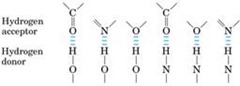
 La interacción es entre moléculas en los organismos vivos, ya sea, entre un grupo hidroxilo de un alcohol con el agua, entre carbonilo de una cetona y el agua, entre cadenas polipeptídicas, entre las bases nitrogenadas que forman parte del DNA estabilizando su estructura, aunque sean débiles pero la suma de ellas es la que cuenta.
La interacción es entre moléculas en los organismos vivos, ya sea, entre un grupo hidroxilo de un alcohol con el agua, entre carbonilo de una cetona y el agua, entre cadenas polipeptídicas, entre las bases nitrogenadas que forman parte del DNA estabilizando su estructura, aunque sean débiles pero la suma de ellas es la que cuenta. Entonces sabiendo los grupos funcionales se puede saber cuan fácil van a interaccionar con el agua.
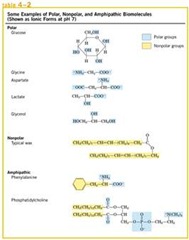
La glucosa tiene muchos puntos polares, muchos grupos hidroxilo que fácilmente pueden formar puentes de hidrogeno con el agua y por lo tanto esta molécula es altamente soluble en agua.
La sacarosa que tiene glucosa y fructosa, que es otra azúcar que tiene grupos OH altamente solubles (cuando ponemos azúcar al te nos damos cuenta).
La glicina es un aminoácido que también tiene grupos polares cargados parcialmente positivos. El Aspartato es otro aminoácido, lo mismo para el lactato glicerol, son todas altamente polares, que pueden formar puentes de hidrogeno.
Con las moléculas que tienen grupos no polares, como las ceras, son muy poco solubles en agua.
Hay moléculas que son relativamente anfipáticas, que tienen una parte apolar mientras que en el otro extremo tienen una parte polar para interaccionar con el agua, y con eso se las arreglan para ser parcialmente solubles, por ejemplo la Fenilalanina.
Luego está la familia de los lípidos, la fosfatidilcolina es un triglicérido, tiene una parte polar pero también una gran parte apolar.
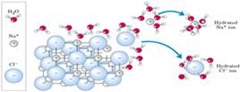
Las sales en general son altamente solubles en agua, puesto que son extremadamente polares, interaccionan fácilmente con el agua porque tienen carga y el anión proviene de un acido fuerte por lo tanto estos son extremadamente solubles en agua.
Los gases también son solubles en agua, pero lo son en la medida en que tienen cargas parciales, sulfuro de hidrogeno que es parecida a la molécula del agua por tanto también tiene una carga parcial negativa por el azufre por su electronegatividad. Uno de los problemas del nitrógeno por ejemplo es que a medida que aumenta presión es más soluble.
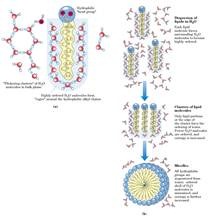
Los lípidos son problemáticos para las soluciones acuosas puesto que tienen una cola que es altamente hidrofóbica que no interactúa con las moléculas de agua y por lo tanto estas moléculas tienden espontáneamente a formar micelas donde exponen la cara polar hacia el agua y dejan en el centro una zona apolar, forman bicapas lipídicas, esto ocurre a expensas de que el agua está muy ordenada alrededor de las moléculas y a medida que se van asociando las moléculas de lípidos, la cantidad de agua alrededor va en aumento, por lo tanto es un fenómeno en el cual la fuerza motriz es la entropía que esta de acuerdo con la segunda ley de la termodinámica.
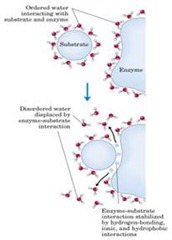 Muy importante es la interacción entre las moléculas como por ejemplo una enzima y su sustrato, la que radica en la formación de puentes de hidrogeno, de nuevo es lo mismo que ocurre con los lípidos. En la imagen vemos que el agua esta ordenada alrededor del sustrato para que el sustrato sea altamente soluble y normalmente es polar por lo tanto el agua esta interaccionando pero al interaccionar se ordena, lo mismo ocurre con la molécula de proteína, una enzima es una proteína, tiene grupos polares por fuera, el agua esta ordenada pero tiene grupos capaces de formar puentes de hidrógeno y otros enlaces débiles y tiene que haber una interacción entre el sustrato y la enzima, para que ello ocurra se desplaza el agua.
Muy importante es la interacción entre las moléculas como por ejemplo una enzima y su sustrato, la que radica en la formación de puentes de hidrogeno, de nuevo es lo mismo que ocurre con los lípidos. En la imagen vemos que el agua esta ordenada alrededor del sustrato para que el sustrato sea altamente soluble y normalmente es polar por lo tanto el agua esta interaccionando pero al interaccionar se ordena, lo mismo ocurre con la molécula de proteína, una enzima es una proteína, tiene grupos polares por fuera, el agua esta ordenada pero tiene grupos capaces de formar puentes de hidrógeno y otros enlaces débiles y tiene que haber una interacción entre el sustrato y la enzima, para que ello ocurra se desplaza el agua.¿Por qué se desplaza el agua?
Porque tiende a formarse enlaces débiles, enlaces puentes de hidrógeno, iónicos e interacciones hidrofóbicas porque algunos grupos de arriba de la proteína también presentan características hidrofóbicas, entonces se desplaza el agua, hay mas moléculas de agua desordenada y la tendencia química por una fuerza de entropía de nuevo es la formación de estos enlaces, pero como son puros enlaces débiles esto es altamente reversible. Entonces tenemos una sumatoria de enlaces débiles entre las moléculas y que son claves para todas las acciones biológicas, esa es una de las características que las interacciones ocurren en general por la formación de enlaces débiles, lo cual le da mucho dinamismo al sistema biológico. La interacción de una hormona con su receptor en general de nuevo predominan las fuerzas débiles lo cual implica que la hormona se puede unir pero también se puede soltar fácilmente y eso explica porque las acciones hormonales duran un determinado tiempo y no se queda pegado puesto que si no quedaría siempre activado el sistema y todos los sistemas de señalización que usan las células que usan los tejidos dependen de estos enlaces débiles que se pueden formar pero también se pueden romper fácilmente.
Entonces tenemos:
v Interacción formando puentes de hidrogeno
v Interacciones iónicas entre dos grupos cargados, también se tiende a pensar que la repulsión no es un tipo de interacción, pero la repulsión es una interacción negativa y es importante para mover a la molécula hacia otro lugar. El que dos grupos tengan repulsión hacen que se orienten dos moléculas de manera distinta, la mantiene alejada de una cierta posición lo que favorece que interaccione con otros grupos.
v Interacciones hidrofóbicas, en donde el agua repele aquellas partes de las moléculas que no tienen grupos polares, por lo tanto hay desorden de moléculas de agua y por lo tanto eso genera que los grupos hidrofobicos tiendan a juntarse, porque al juntarse hay menos moléculas de agua a su alrededor que mueven en cierto sentido a las moléculas.
v Fuerzas de Van der Waals, son las más débiles y que son interacciones por proximidad. Pues a cierta distancia los átomos se atraen.
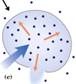
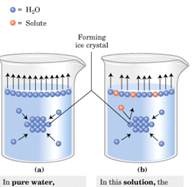 Otra característica del agua es que sus características varían cuando tienen solutos incorporados y como se ve en la figura todas las moléculas están expuestas en su superficie y la presión de vapor tiene un valor determinado, sin embargo en una solución no todas las moléculas son de agua sino que también hay solutos (en rojo), por lo tanto la posibilidad de salida de escaparse de la solución a la fase gaseosa es menor y la presión de vapor tiende a disminuir y por otra parte la tendencia a formar cristales de agua también tiende a disminuir en una solución que en agua 100% pura.
Otra característica del agua es que sus características varían cuando tienen solutos incorporados y como se ve en la figura todas las moléculas están expuestas en su superficie y la presión de vapor tiene un valor determinado, sin embargo en una solución no todas las moléculas son de agua sino que también hay solutos (en rojo), por lo tanto la posibilidad de salida de escaparse de la solución a la fase gaseosa es menor y la presión de vapor tiende a disminuir y por otra parte la tendencia a formar cristales de agua también tiende a disminuir en una solución que en agua 100% pura.La solución acuosa incorporada en nuestras células es una solución con características muy especiales pues tiene una altísima concentración de soluto la presión de vapor y la formación de cristales no es exactamente igual lo que hace que organismo vivos puedan vivir a -1 a -2 º C sin que se congelen.
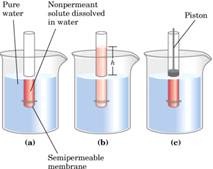 Otro efecto de las soluciones acuosas es que cuando están separadas por una membrana semipermeable como es lo que ocurre en la célula que tienen un medio acuoso en su interior y están rodeadas de un medio acuoso, si la concentración de la solución es distinta a un lado de otro el agua tiende a moverse con el fin siempre de diluir la solución que esta dentro del tubo, entra agua y aumenta el volumen en el fondo tratando de que se equiparen ambas concentraciones y luego si manipulamos un pistón ejercemos una fuerza para llevarlo al volumen original lo que se conoce como presión osmótica, así se mide.
Otro efecto de las soluciones acuosas es que cuando están separadas por una membrana semipermeable como es lo que ocurre en la célula que tienen un medio acuoso en su interior y están rodeadas de un medio acuoso, si la concentración de la solución es distinta a un lado de otro el agua tiende a moverse con el fin siempre de diluir la solución que esta dentro del tubo, entra agua y aumenta el volumen en el fondo tratando de que se equiparen ambas concentraciones y luego si manipulamos un pistón ejercemos una fuerza para llevarlo al volumen original lo que se conoce como presión osmótica, así se mide.Es importante en los seres vivos puesto que tienen que tener una concentración de solutos muy parecidas en el interior de la célula y en exterior de la célula, una concentración total porque no son iguales ( la concentración de proteínas es muy parecida adentro y afuera porque por ejemplo dentro de la célula hay mucho mas potasio y fuera hay mas sodio), la osmolaridad externa e interna es mas o menos la misma y por lo tanto no hay movimiento neto de agua al interior o al exterior de la célula, lo que no quiere decir que no entre agua ni salga agua, entra y sale en la misma cantidad. Las células poseen un equilibrio dinámico de fase estacionaria, no hay cambios medibles.
Medio hipertónico (osmolaridad mayor afuera) sale agua de la célula y se arrugara.
Medio hipotónico, entra agua a la célula y se hinchara hasta romperse.
 Por ejemplo si se centrifuga la sangre a baja velocidad, luego se puede separar los glóbulos rojos del sobrenadante que será pálido o incoloro pero si colocamos a los glóbulos rojos en agua estos se hincharan hasta romperse entonces por más que centrifuguemos siempre tendremos una única solución roja pues los glóbulos rojos liberaron su contenido al medio.
Por ejemplo si se centrifuga la sangre a baja velocidad, luego se puede separar los glóbulos rojos del sobrenadante que será pálido o incoloro pero si colocamos a los glóbulos rojos en agua estos se hincharan hasta romperse entonces por más que centrifuguemos siempre tendremos una única solución roja pues los glóbulos rojos liberaron su contenido al medio.Los movimientos de las hojas tienen que ver con cambios en la tonicidad del tejido vegetal y la gracia es que además de su membrana celular tiene una pared rígida y por lo tanto se pueden dar el lujo de cambiar la osmolaridad del medio externo haciéndolo hipertónico o hipotónico y pueden entrar agua a la célula o salir, si entra agua la célula no se rompe por la presencia de la pared pero si aumenta la presión dentro y como consecuencia la planta está turgencente ( comparemos una ramita de apio, cuando este blanda agregarle agua y se verá que después está más dura). En la foto se ve que la planta puede cerrar sus hojas por lo dicho anteriormente.
Otra propiedad del agua es que al ser una molécula que presenta polaridad parcial negativa y positiva, tiene la capacidad de disociar, y puede disociar un protón y liberar un grupo OH- y por lo tanto el agua presenta un pH que puede ser modificado dependiendo de los componentes que tenga disueltos. El pH normal del agua pura es de 7. El pH sanguíneo normal es 7.4 a 6.5 estamos muertos y 7.8 también o sea vivimos en un pH estable, lo que se llama capacidad amortiguadora.
¿Qué es un amortiguador?
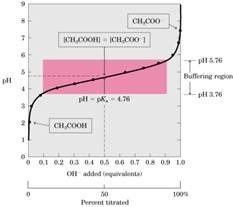
El profesor lo explica a través de un ejemplo con el acido acético. Es un acido débil lo que significa que la especie que predomine en solución (ya sea acido acético como tal o su base conjugada) va a depender exclusivamente del pH al que nos encontremos. Hay zonas donde se pueden agregar protones y el pH varia poco, y esa es la zona donde es capaz de amortiguar los cambios de pH una sustancia en particular.
Hay un punto medio en particular en donde la cantidad de acetato y acido acético es igual, vale decir tanto los compuestos ácidos y los como los básicos se igualan y ese punto se conoce como el pKa (logaritmo negativo de la constante de equilibrio) y para este en particular el pKa = 4,76.
¿Cómo se puede calcular ese punto?
Se registra el pH y luego con la 1º derivada y luego la 2º y a continuación aparece un punto de inflexión el cual nos indicara exactamente cuál es el pKa.
Entonces la capacidad tamponante de una sustancia se considera que es más o menos una unidad de pH alrededor de su pKa, y lo que tiene que ver es con el rango donde está en juego la disociación de este compuesto.
Ecuación de Henderson- Hassel-Balch.
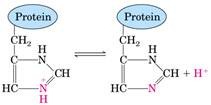
Tenemos una proteína con un grupo funcional amino que puede disociarse y por lo tanto se comporta como base débil por lo tanto aporta protones y también puede aceptar protones por lo tanto puede participar en la regulación del pH.
El CO2 de nuestra respiración lo manejamos como bicarbonato y su disociación está aportando protones.
Es necesario recalcar que el juego de protones y la mantención del pH es fundamental para los sistemas biológicos y es además muy dinámico por lo demás.
Por otra parte el pH es muy importante para la actividad biológica, los siguientes son los pH donde trabajan mejor las enzimas mencionadas en el grafico.
La pepsina que es una proteasa que trabaja en el estomago a un pH muy bajo y en el intestino su optimo de funcionamiento es a pH acido. La tripsina que está orientada a trabajar en el intestino a un pH que es el del intestino. La fosfatasa alcalina solo esta puesta como curiosidad y el profe no le da mayor importancia.











0 comentarios:
Publicar un comentario