En química orgánica normalmente se conoce los grupos funcionales (Ácido Carboxílico y amino), y se escribe el aminoácido en su forma no iónica con los grupos funcionales no ionizados tal cual.
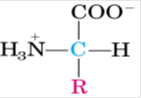 En bioquímica es más común escribir la estructura del aminoácido con su forma mayoritaria (la estructura iónica mayoritaria del aminoácido cuando está en solución acuosa, porque ahí este grupo acido carboxílico esta desprotonado y el grupo acido alfa amino esta protonado y tiene un carácter básico por lo tanto tiende a captar protones del medio; esta forma es la del switter-ion (switter significa dos cosas contrapuestas en la misma estructura , una carga positiva y una negativa en la misma molécula ) esta forma es la más usada.
En bioquímica es más común escribir la estructura del aminoácido con su forma mayoritaria (la estructura iónica mayoritaria del aminoácido cuando está en solución acuosa, porque ahí este grupo acido carboxílico esta desprotonado y el grupo acido alfa amino esta protonado y tiene un carácter básico por lo tanto tiende a captar protones del medio; esta forma es la del switter-ion (switter significa dos cosas contrapuestas en la misma estructura , una carga positiva y una negativa en la misma molécula ) esta forma es la más usada.(En la prueba si pregunta por una carga en una cadena lateral, ella no pondrá la estructura ionizada sino simplemente el grupo funcional y corre por nuestra cuenta saber si esta desprotonado)
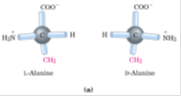
En la parte estereoquímica, se toma de ejemplo un aminoácido: la L-alanina que es uno de los aminoácidos comunes o estándar que tiene como cadena lateral un metilo, se señala la estereoquímica de éste, cuya configuración es la siguiente: distribución espacial con el C asimétrico, 2 enlaces hacia hidrógenos y hacia el grupo alfa amino hacia delante, por lo tanto C es tetraédrico, los otros enlaces los tiene hacia atrás.
El otro isómero óptico es la D-alanina en el que se mira el C con los 2 enlaces hacia atrás, pero hacia la izquierda está el protón y hacia la derecha el amino, por lo tanto la D-alanina, es un isómero óptico de la L-alanina, es otro compuesto, otro isómero.
Lo importante es que todos los aminoácidos comunes estándares que están en las proteínas son el isómero L no el D.
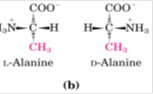
Las proyecciones de Fisher
Son muy usadas por lo que se estableció una conversión que consiste en que los derivados de compuestos que tienen acido carboxílico éste se coloca arriba, después en la cadena vertical el C asimétrico va al centro y los enlaces hacia el lado son los enlaces que van hacia delante y el grupo ubicado por la izquierda acepta el amino.
Si no hubiese esta conversión de por medio podría no ser proyección de Fischer, pero cuando se dibuja de esta manera se está pensando en ello, por lo tanto es otro compuesto.
Existen 20 aminoácidos comunes todos codificados en el código genético y presentes en todas las especies vivas, porque usan los mismos aminoácidos para sus proteínas, estos aminoácidos tienen abreviaturas para nombrarles; existe un código de 3 letras, por ejemplo la glicina se abrevia GLY, la alanina, ALA, etc.
Este código es práctico porque se reconoce rápidamente el aminoácido.
Además existe un código de una sola letra aquí la glicina también es G, sin embargo existen muchas letras que se repiten, por ejemplo alanina es A, en cambio asparragina es M porque la A ya está ocupada , este código no es tan fácil de recordar, las personas que lo manejan es porque lo saben, pero es bueno saber que una sola letra representa un aminoácido, este código es útil cuando se quiere informar la secuencia de una cadena polipeptídica relativamente larga porque uno pone una letra tras otra y sale más corta.
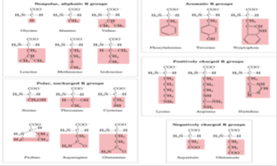
Aminoácidos común estándares agrupados (se estudiaran según el grupo R que es la variable)
Grupo R no polar alifático (no aromático):
Forman parte de este grupo:
La glicina cuya mayor importancia es ser el único aminoácido que no tiene 2 isómeros ópticos debido a no poseer un carbono asimétrico (es el aminoácido más pequeño).
La alanina (posee metilo en cadena lateral).
La valina (con 3 C).
La leucina (4 C)
La isoleucina (4 C, pero la cadena lateral es un isómero de su otra cadena).
Las cadenas laterales de la leucina e isoleucina son las cadenas laterales mas apolares, aunque también lo es la cadena de la valina.
Polaridad se refiere a cargas netas o parciales, en cambio apolar carece de lo anterior, esta característica sin embargo es exactamente igual para la alanina y leucina porque no tienen carga neta ni parcial, entonces ¿por qué son más apolares que la alanina la isoleucina y la leucina? Se hace una analogía con efecto hidrofóbico, este efecto en las cadenas laterales es más pronunciado porque de ser apolar obviamente la alanina también lo es, pero el efecto hidrofóbico es más pronunciado cuando el grupo es más grande.
¿Cuál es la cadena mas apolar?
No es la alanina porque esta es más chiquita.
La Metionina tiene la gracia de tener azufre (solo 2 aminoácidos tienen azufre) en un grupo funcional, el S es característica similar al oxigeno, por ende este grupo funcional será tío éter porque es análogo al éter, entonces si se analiza el S (un heteroátomo) nos damos cuenta que no tiene electronegatividad idéntica al C, pero este tipo de grupo funcional, éter es un solvente apolar que no aporta mayor polaridad, (además el S es diferente del oxigeno).
Grupo R aromático
La Fenilalanina que tiene el metilo sustituido por un fenilo, es un grupo R apolar.
La tiroxina es la Fenilalanina con un grupo hidroxilo y su cadena lateral es aromática pero no apolar porque el grupo hidroxilo interacciona con el agua.
El benceno con un hidroxilo originan el fenol, (es un grupo fenólico).
La tiroxina tiene en su cadena lateral un grupo fenólico y el fenol tiene características de acido débil, también el OH de la tiroxina es débilmente acídico, es decir, la tiroxina en ambiente acuoso tiende a ceder un protón, se libera quedando una carga negativa. Justamente la característica de ser débilmente acídica, la poseen los compuestos que tienen un OH sobre un anillo aromático, porque un hidroxilo de un alcohol común y corriente no lo es, lo mismo sucede con el propanol, el metanol, porque si uno los mezcla con agua y mide el pH este será de 7, es decir, el H de un hidroxilo de un alcohol común y corriente no es acídico, pero un fenol en agua si lo es.
¿Por qué un hidroxilo sobre un anillo aromático tiene carácter de acido? ¿Por qué el grupo funcional ácido carboxílico es un acido siendo que el hidroxilo que también tiene un H no es acido?
En el acido carboxílico cuando se desprende un H la carga negativa que da se puede deslocalizar (resonancia) por eso el anión es relativamente estable, en cambio en el caso del etanol si se desprende el H el anión no tiene donde ir, entonces es inestable.
La tiroxina es débilmente acídica, se pueden unir grupos fosfatos que tienen una cierta reactividad en algunas proteínas existentes.
El triptófano, tiene un anillo de 4 C, uno de 5 con un N (es un anillo indólico), lo que le da la característica de aromático son los 2 anillos y es el sistema más grande de las 3 cadenas laterales.
El triptófano es el aminoácido de PM más alto, posee la cadena lateral más grande de todos los aminoácidos comunes.
Lo más interesante de los aminoácidos con cadena lateral aromática es su capacidad para absorben luz ultravioleta siendo el triptófano el que más absorbe de los 3(la tirosina y la Fenilalanina en menor cantidad), por ejemplo si una proteína tiene aminoácidos aromáticos la que tenga más triptófano va a absorber más luz UV, en general se usa esta característica para detectarlas cuando se están preparando.
Cadena lateral polar pero no cargada como grupo R.
La serina y la treonina tienen aminoácido con hidroxilos en su cadena lateral, estos hidroxilos pueden formar puentes de H con agua por lo que participan en la solvatación de las proteínas, permiten que estas queden solubles por ejemplo, además cerina y treonina pueden ser sustituidas por fosfato, porque hay cierta reactividad del grupo hidroxilo, a su vez también se pueden unir cadenas azucares.
Cisteína es un aminoácido único porque tiene un grupo tiol o sulfhidrilo, se nombra como sulfhidrilo de la cisteína, (éste es el segundo aminoácido que tiene S) ésta cisteína forma puentes disulfuro por eso su importancia.
Prolina también tiene algo único entre los 20 aminoácidos debido a que tiene su grupo alfa-amino integrado a un ciclo y eso no ocurre en los otros aminoácidos (pues lo tienen siempre libre), esto hace que las posibilidades de rotación en los enlaces sean restringidas, lo que hace que sea importante en la estructura que puede adoptar la proteína que tiene prolina en alguna posición. (Su cadena lateral no es polar sino apolar).
Cuando el grupo amino forma parte de un ciclo es un grupo imino entonces la prolina es un iminoácido.
Asparragina y glutamina también son de este grupo, pues tienen el grupo funcional amida en la cadena lateral que le permiten formar puentes de hidrogeno y así participar en la solvatación de las proteínas.
Grupo R cargado positivamente,” los aminoácidos básicos”.
Es el termino más común para referirse a estos aminoácidos y son los que tienen el grupo de características básicos en su cadena lateral, el grupo básico de los compuestos orgánicos es el grupo amino.
La lisina (con una cadena lineal y un grupo amino), los compuestos que tienen grupo funcional ácido Carboxílico el C alfa-amino se pone en el lado beta, gama, Épsilon, y se nombra por ejemplo el grupo E amino de la lisina.
El grupo alfa amino y el grupo E amino de la lisina se diferencia en que tiene 2 grupos aminos.
Se llama básico porque predomina este carácter y tiene un solo acido (grupo).
Arginina tiene 3 N con estructura tipo guaranina.
Histidina con estructura cíclica con N en su cadena lateral, es un grupo funcional imidazol.
En este grupo no sólo se ve la carga positiva, sino que también se muestra para pH 7 por las estructuras iónicas características de basicidad que tiene este grupo a tal pH.
Aminoácidos con carga negativa en la cadena lateral.
Aspartato y Glutamato con una cadena un poco más larga se les llama también acido aspartático y acido glutámico.
Hay dos grupos funcionales ácidos y uno básico.
¿Cómo se forma un puente disulfuro?
Dos moléculas de cisteína reaccionan y se forma el puente disulfuro, es un enlace covalente (es el único aparte del peptídico que se puede establecer entre aminoácidos en las proteínas, entre los aminoácidos comunes)
El tipo de reacción producida cuando se forma el puente disulfuro químicamente es una redox y dentro de ésta, en el sentido izquierda-derecha, ocurre una oxidación porque cede electrones por un agente oxidante como oxigeno del aire, en cambio, para romper un puente disulfuro se usa un agente reductor.
Los aminoácidos no estándares o aminoácidos modificados
Se pueden encontrar al analizar la composición de una proteína, son menos comunes ya que pocas las que los contienen y si una llegara a tenerlo sería entre 1 o 2.
Se forman por modificación de un aminoácido común, por ejemplo la 4-hidroxi-prolina se forma cuando la prolina se hidroxila en su carbono 4.
Los aminoácidos modificados se forman después de la síntesis de la cadena polipeptídica, es una modificación post-tradicional ya que primero se sintetiza la cadena polipeptídica y luego una enzima introduce las modificaciones.
Ejemplo la hidroxiprolina es fundamental en el colágeno que está en la membrana basal y también en la piel, huesos (matriz), ligamentos, para que ocurra la hidroxilación se requiere vitamina C entonces en el escorbuto cuando no hay esta vitamina el colágeno se empieza a romper y ocurre la enfermedad.
Otros aminoácidos modificados, la 5 hidroxilisina (lisina con hidroxilo), 6-metil-licina, o sea en el nitrógeno que esta sobre el C 6 está el metilo.
Estos aminoácidos modificados no están codificados en el genoma, sino que lo está el aminoácido común y luego se produce la modificación, después de la traducción.
Propiedades acido-base de los aminoácidos
Cuando están en solución conducen corriente eléctrica
Para el tema de las protonaciones o no protonaciones hay que recordar la escala de pH, con un 7 corresponde a una (H) 1.0X10-7 y los más bajos son los acídicos porque la concentración de H es más alta y lo contrario son los básicos.
pH= -log (H) el pOH no se utiliza
(El grupo alfa amino protonado también es un acido débil.)
Dentro de los ácidos débiles no todos son iguales respecto a que tan débiles son, eso se expresa a través de la constante de acides Ka.
¿Cómo se sabe cual acido es más fuerte?
R: Cuando Ka es más alta, más fuerte es el acido débil.
En bioquímica no se usa el Ka sino que el pKa y se define como:
–log Ka = pKa donde un menor pKa indica mayor acidez.
Esta ecuación se usa para calcular el pH de una solución tampón, si uno tiene un compuesto con características de acido débil con un cierto pKa en un ambiente celular con un cierto pH, conociendo el pKa del acido débil uno puede saber si esta protonado o no.
Si el grupo estuviera al pH igual que al pKa (numéricamente) lo que sucede es que ambas concentraciones serán cero, entonces si el pH es igual al pKa el acido débil esta en el punto medio de su equilibrio de protonación / desprotonación, es decir la mitad del acido débil esta desprotonado y la otra mitad no lo está, en cambio si el pH fuera una unidad menor que el pKa entonces tiene que haber más concentración de HA que de A- por ejemplo (10 veces más) y si el pH fuera 2 y el pKa 4 seria 100 veces mayor.
Comparando el pH con el pKa se puede dar cuenta que sucede con un determinado grupo a ese pH, en cambio la Ka da la misma información, pero hay que realizar más cálculos.
Ejemplos ilustrados
Escala de pH con ácidos débiles, un acido monotrópico por ejemplo acido acético y se pone el equilibrio de protonación en el que su H esta encima del pH para simbolizar esto el ácido acético esta a pH 4.76 (esta la mitad protonada y la otra no), en cambio amonio es acido conjugado del amoniaco que es una base orgánica. (Entonces el amonio es un acido débil.)
Se indica el pKa del acido conjugado de la base débil, no se informa el pKb de la base débil, en bioquímica nunca se toman en cuenta los pKb, siempre se manejan los pKa de los grupos ácidos, ácidos Carboxílicos y amino protonado.
Ejemplo otros
Acido Fosfórico con 3 diferentes protones, entonces cuando se disocia el primero el pKa es 2.14 acido fuerte, el segundo pKa 6.86, el del H2PO4- y el HPO4-2con sus cargas negativas, eso permite separar los tampones.
Volviendo a los aminoácidos, existen 3 diferentes especies iónicas de glicina a un pH muy acido, y su grupo acido Carboxílico no estará desprotonado, el alfa-amino si estará protonado.
Lo que primero se disocia si uno aumenta el pH (al titular con una base) es el protón del acido Carboxílico, a un pH mas alcalino un protón se desprende y se queda con otra especie.
Hay 3 tipos de especies iónicas y dependiendo del pH hay más de uno o más de otro, es un equilibrio químico, así que teóricamente siempre están las 3 presentes solamente en distintas concentraciones.
Dibujo curva de titulación
Si uno tiene solución de glicina a un pH muy acido y se empieza a titular con NaOH aumenta el pH (se hace mas alcalino), se llega a una zona donde el pH cambió poco al agregar NaOH (tampón), después cambia violentamente. Lo más interesante de esto es el punto isoeléctrico, que se refiere a la idea de que tiene que haber un pH en el cual la estructura que tiene una carga neta de cero sea la mayoritaria y la concentración de esta especie iónica con carga neta +1 sea igual a la concentración de la especie con carga neta cero y si se hiciera un balance a ese pH, la carga neta seria igual a la negativa y se anulan entonces ese pH al cual la carga neta de un aminoácido es cero es el punto isoeléctrico (es un pH al cual la carga neta es cero, cuando se anulan las cargas netas con cargas)
¿Cómo se calcula el punto isoeléctrico?
R: Se suman los pH, es el promedio.
Ejemplo 5.97 que es el promedio de 9.6 y 2.34. Así se calcula el punto isoeléctrico de un aminoácido que no es acido ni básico como glicina o alanina (los 2 valores se promedian).
El concepto del punto isoeléctrico también existe para proteínas, los péptidos tienen punto isoeléctrico, las proteínas todos los compuestos que tiene carga negativa y cargas positivas (anfóteros) por ejemplo el acido Acético no tiene punto isoeléctrico porque no tiene carga positiva solo negativa.
Cuando la carga neta es cero no migra en un campo eléctrico (no se mueve), esto tiene relación con la electroforesis, un tipo de cromatografía (la de intercambio iónico) que permite separar aminoácidos, etc.
Siendo que el punto isoeléctrico es 5.97 si el pH es 4 ¿Qué tipo de carga neta tendrá la glicina? (No numéricamente) será positiva entonces si el pH es menor la carga es positiva, si es mayor es negativa.
Si es más diferente el punto isoeléctrico mas diferenciado será esto.










0 comentarios:
Publicar un comentario